回看人类与癌症抗争的漫长历史,手术刀算得上古老的武器之一。随着科学的进展,化疗、靶向治疗、免疫治疗等“新式武器”也不断涌现。但尽管如此,在抗击胃癌的战场上,外科手术仍然保有其重要地位,尤其对于早期和进展期的胃癌来说。
胃镜手术:“精细化”管中取瘤
对大部分癌症来说,“早发现、早治疗”是提升治愈率的重要因素,于胃癌而言尤其如此。因为“早期”就意味着肿瘤体积小,未转移,有望通过一些损伤小的方法来实现治愈。在胃癌治疗中,胃镜手术就扮演着这样的角色。

(内镜检查)
胃镜有着非常大的应用灵活性,不仅可用内镜取标本做活检,还可进行手术。但由于胃癌易转移到胃周围的淋巴结,而这些淋巴结转移灶难以用内镜清扫,因此胃镜手术的适用范围相对较窄。
那么,哪些胃癌是胃镜手术的绝对适应证呢?答案是:组织学类型分化良好,大小在2厘米以下的非溃疡型,同时分期属于cT1a的黏膜内早期胃癌[1]。而除去绝对适应证外,还有一部分扩大适应证:① 2厘米以上非溃疡型、组织类型分化良好cT1a;② 3厘米以下的溃疡型、分化性cT1a;③ 2厘米以下非溃疡型、未分化型cT1a,无脉管侵犯的情况下,淋巴结转移危险性较低,可扩大适应证范围。
具体到操作方法,胃癌的胃镜手术主要有内镜下黏膜下层剥离术(ESD)和内镜下黏膜切除术(EMR)两种。其中,ESD的适用范围更广,也是目前国内外普遍使用的标准治疗方法[2]。
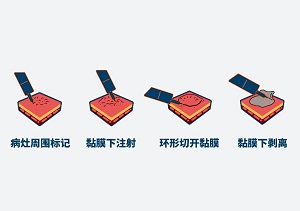
(ESD治疗步骤)
那么,ESD的治疗步骤是怎样的?首先,需要在胃镜下找到要切除的病灶进行标记;然后在病灶下注射液体,把黏膜层的病灶抬起,从而和肌层分离;接下来,则会切开病灶周围的黏膜,再剥离掉病灶部位;最后一步,是对剥离的部位进行止血处理。
虽然胃镜手术创伤小,但由于其手术范围有局限,有时不一定能将肿瘤切除干净,所以患者在胃镜手术后需遵医嘱进行随访。如术后病理检查结果显示病灶切除不彻底,就需要继续追加治疗,比如再做ESD一次,或者直接进行开腹手术[1]。
在中国,早期胃癌患者占比不到20%[3],许多患者确诊时已是进展期。这种情况下,若患者的身体条件可以接受手术,就轮到外科手术登场了。
外科手术:“大开大合”斩除病灶
相较于胃镜手术,外科手术在胃癌治疗中的适应证范围要大得多。拿根治性手术来说,临床分期在I期到III期,甚至部分IV期的胃癌患者,一般都可接受手术。当然若患者有特殊情况,比如存在身体虚弱,或凝血功能差等问题,则可能不适宜进行手术。
标准的胃癌手术,要求切除的胃部体积占到整个胃的2/3以上。依据肿瘤位置的不同,切除的范围也会有变化。较常见的做法是切除远端胃或整个胃。
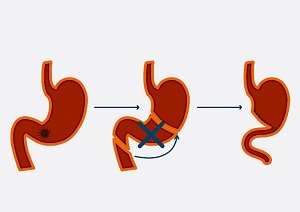
(胃癌切除三部曲)
如上文提到的,胃癌经常通过胃周围丰富的淋巴结进行转移,因此清扫这些淋巴结也是手术的重要部分。同时,淋巴结转移的状况也是胃癌分期很重要的参考因素,所以目前国际通用的第8版胃癌分期中,明确要求手术中至少切除16枚淋巴结进行病理检查[2]。
淋巴结清扫的范围也需根据切除胃的范围来确定。一般情况下,要求清除胃癌转移的前两站淋巴结,包括胃周围、肝、脾、胃左动脉附近的淋巴结等。这就是所谓的D2根治手术,目前在中国和日本等亚洲国家被广泛使用[2]。
完成胃和转移淋巴结的切除后,还有一项重要的工作就是重建消化道。胃在人体的消化系统中有重要的作用。因此,如何在术后保证患者的基本消化系统功能是非常关键的。消化道重建的方式,则需要依据胃的切除范围来选择[3]。
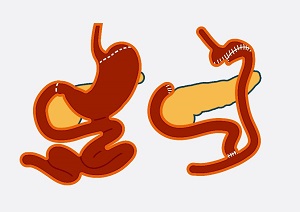
(胃癌切除术后重建消化道)
晚期胃癌患者如果出现胃梗阻、出血、疼痛、营养不良等症状,也可考虑通过手术进行缓解。如做造口、胃和空肠吻合、姑息性切除等。但遗憾的是,非根治性的减瘤手术已被证实无法延长患者的生存期,只能改善部分症状[4]。
高质量的外科手术治疗,目前仍是实现治愈胃癌目标的重要力量,它与术前术后联合(放)化疗的协同合作也正为患者创造更多治愈可能。
而在免疫治疗时代,多项临床研究也正在探讨免疫治疗用于围手术期治疗的可行性,包括用于手术后杀灭残余癌细胞,降低复发风险的辅助性治疗和在手术前用于缩小肿瘤,降低手术难度,提高切除成功率的新辅助性治疗[5]。
免疫治疗的入局,可能会让手术患者围手术期的治疗模式迎来积极改变,不过用药模式、剂量等问题还有待临床试验的探索。考虑到胃癌发生机制的复杂性与复发转移的高风险性,治疗的过程中还是需要遵照医嘱,因人而异选择适合的方式,才有可能实现对胃癌精准有力的打击。
参考资料:
[1] 中国临床肿瘤学会胃癌诊疗指南,2018V1.
[2] Smyth E C, Verheij M, Allum W, et al. Gastric cancer: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up[J]. Annals of Oncology, 2016, 27(suppl_5): v38-v49.
[3] 中华人民共和国国家卫生健康委员会,《胃癌诊疗规范(2018年版)》.
[4] Fujitani K, Yang H K, Mizusawa J, et al. Gastrectomy plus chemotherapy versus chemotherapy alone for advanced gastric cancer with a single non-curable factor (REGATTA): a phase 3, randomised controlled trial[J]. The Lancet Oncology, 2016, 17(3): 309-318.
[5] Terashima M, Kim Y-W, Yeh T-S, et al. 778TiPATTRACTION-05 (ONO-4538-38/BMS CA209844): a randomized, multicenter, double-blind, placebo- controlled Phase 3 study of Nivolumab (Nivo) in combination with adjuvant chemotherapy in pStage III gastric and esophagogastric junction (G/EGJ) cancer[J]. Annals of Oncology, 2017, 28(suppl_5), mdx369.160.
文章及图片版权归“给生命以时光”消化道肿瘤疾病教育项目主办方和支持方所有。











