作者:顾思超
单位:国家呼吸医学中心 中日友好医院呼吸与危重症医学科
本文将从必要性、可行性和风险性三方面评估重症COVID-19患者ECMO的辅助治疗。必要性指患者实施ECMO的适应证是否强烈,有无其他替代手段。可行性指患者是否有条件做ECMO。此外,实施ECMO之前一定要评估患者当前存在的风险。任何有创操作的风险性和必要性都存在相互交叉,在必要性和风险性之间如何平衡,这也是临床医生面临的重要问题。

一、ECMO的必要性
ECMO是整个呼吸支持的最后一道防线,如果患者低氧情况非常严重,需要通过ECMO予以纠正。对于ECMO的介入时机尚未达成共识。部分学者主张及早介入,还有部分学者提倡根据既往研究,将氧合指数或二氧化碳水平升高作为判断指标。
2022年发表的一项研究虽然与ECMO的关系不大,但也提示我们,如果在早期纠正低氧,患者可能会获益[1]。该研究分为两组,第一组早期插管、吸氧≤6 L/min的患者;第二组为延迟插管,吸氧>6 L/min,HFNO、NPPV的患者。经过统计分析发现,两组患者的氧合在插管前并无显著差异,但早期插管患者低氧纠正得更快,该组患者住院病死率下降。该研究最终也做了一些分析:①因为呼吸驱动过强,低氧过程可能会加重肺损伤;②严重低氧可能对机体的影响较大,尤其是慢性心肺疾病患者,严重低氧可能会继发多脏器功能衰竭。插管后,患者的呼吸驱动、循环和氧合都会得到纠正,使血流动力学更稳定。如果能在更早期纠正低氧,是否能改善COVID-19患者的病死率,值得我们探讨。因此,目前也有一部分学者认为,提早干预低氧可能对患者预后有益,但这必然会面临过度治疗的问题。
目前,常规呼吸支持手段还是从鼻导管吸氧逐渐升级,经过面罩、HFNC、无创通气,如果氧合维持不住,最终需要有创正压通气(IPPV)。从最新发表的《奥密克戎变异株所致重症新型冠状病毒感染临床救治专家推荐意见》[2](以下简称专家意见)也可以看到,通过设定重症患者氧疗目标(SpO2 92%~96%),呼吸支持方式逐层升级,普通氧疗→高流量(首选)→NPPV→IPPV,而且第一次明确了清醒俯卧位在治疗呼吸衰竭中的地位。专家意见还提出应避免气管插管延迟和紧急气管插管。不要使患者低氧持续时间过长,才能改善患者预后。此外,专家意见也推荐了ECMO的应用指征:PaO2/FiO2<100 mmHg【PaO2/FiO2<50 mmHg,超过3 h;PaO2/FiO2<80 mmHg,超过6 h;pH<7.25,PaCO2>60 mmHg,超过6 h】。
如何选择实施ECMO的患者?ELSO指南推荐:PaO2/FiO2<150 mmHg,应考虑开始实施各种辅助治疗,如果采取的措施没有改善患者氧合,尽快实施ECMO。下表是2022年更新内容,可见在不同时期,对患者的选择标准不同。
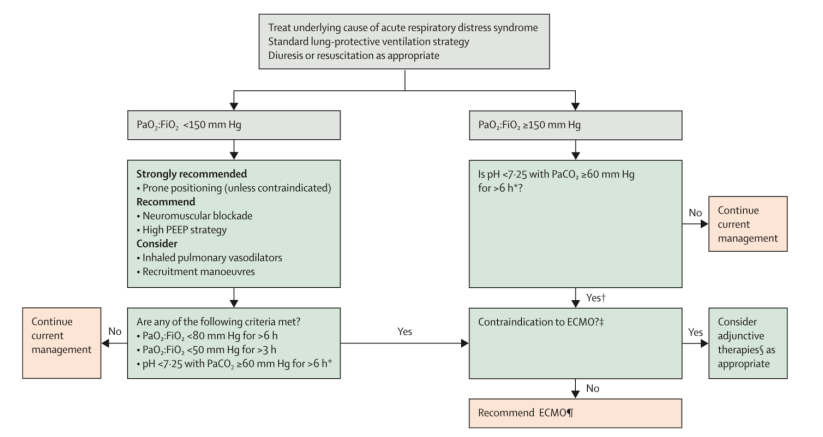
二、ECMO的可行性
对于COVID-19患者,VV-ECMO为主(93%以上),如果是ARDS患者,几乎100%是VV-ECMO。穿刺方法选择超声引导下Seldinger法穿刺,避免了很多血管并发症的发生,但也需要经过一定专业训练的医生操作。美国有一篇文献显示,没有经过训练的胸外科或其他科室医生实施ECMO,并发症明显增加。
多数患者上、下腔静脉扩张,因此在穿刺时通常阻力不大。ELSO指南建议使用23 Fr及以上引流管、19~23 Fr灌注管。其优势是能够达到充分引流。ELSO指南还推荐避免使用单根双腔管作为穿刺首选,因为这种穿刺一般需要影像学定位,需要花费更多时间,患者低氧持续的时间会可能会更长。

三、ECMO治疗的风险性
ECMO的风险性主要从以下几方面考虑:①疾病的可逆性;②抗凝与血栓:如果COVID-19病情没有进展至危重症阶段,抗凝仍需加强,需给予治疗剂量抗凝。一旦进展到ECMO支持阶段,或进展至危重症阶段,需予预防剂量抗凝;③炎症风暴:启动ECMO后,炎症风暴在早期(72 h内)会增强,因为血液与ECMO接触后会产生炎症介质的释放,也有小样本研究显示,COVID-19患者实施ECMO后,炎症风暴还会出现第二次小高峰,在7~10 d左右。所以临床需要警惕,如果建立ECMO 7 d后,患者炎症介质再次升高,可能是ECMO所致,尤其对于COVID-19患者;④导管相关血流感染:COVID-19患者治疗期间使用了大量激素、免疫抑制剂等,淋巴细胞计数可能非常低,加之俯卧位,患者发生导管相关血流感染的风险非常大;⑤新药物在ECMO下的PK/PD:目前这方面的研究数据较少,例如是否需要在ECMO下调整剂量,ECMO对这些药物有无吸附,药物达标情况如何,等,这些问题有赖于更多研究予以解答。本文将主要介绍疾病的可逆性和抗凝与血栓两部分。
1. 可逆性
国外文献报道了一例35岁男性患者,基础合并1型糖尿病,入院第1天胸部CT可见两肺渗出和实变明显,可见牵引性支气管扩张,氧合维持不住,入院第2天行VV-ECMO,常规肝素抗凝,第4天予以托珠单抗,并予地塞米松10 d。第35天,胸部CT可见部分实变有吸收,双肺有纤维化趋势。第90天,撤离ECMO。该患者机械通气共计137 d,160 d转入当地康复中心继续治疗[3]。通过ECMO治疗,患者氧合、通气量、肺顺应性逐渐改善。ECMO在重症COVID-19患者中的可行性究竟如何,仍有待探讨。
重症COVID-19患者发生纤维化的病例仍较多,如果继续维持,首先面临院感问题,其次涉及伦理问题。该患者第112天的胸部CT可见肺部病变有一定吸收,但上肺的纤维化病变仍存在。1年半后,患者上肺纤维化有修复趋势。在重症流感患者中,当ECMO维持60 d左右时,患者可能就会出现类似该患者1年后的影像学变化,后续6个月或1年复查,重症流感患者肺部病变的吸收变化会优于重症COVID-19患者。如果单纯从病毒性肺炎角度出发,COVID-19与流感类似,例如后期都可以出现纤维化,但二者不同之处在于,COVID-19患者肺的纤维化早期出现可能会更多,后期修复的概率可能更低。
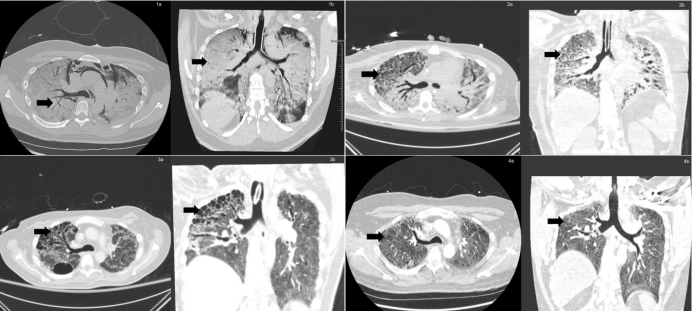
图源:Am J Med Sci, 2022, S0002-9629(22)00492-X.
另一项研究发现,对于绝大多数患者,ECMO平均使用时间为11 d,ICU平均住院时间为40 d,有超过3例的患者ECMO平均使用时间超过100 d[4]。德国一项研究数据显示,ECMO支持超过60 d的患者最终存活了5例,其中1例做了肺移植。如果给ECMO患者充足的恢复时间,他们有机会恢复到较为正常的生活状态,但这种概率极低。大部分数据显示重症COVID-19患者的平均ICU住院时间只有14 d,绝大多数患者还是去世了。此类患者使用ECMO长时间维持,究竟能否恢复,仍未可知。所以,COVID-19是有可逆性的,但需要比重症流感患者更长的恢复时间。
2. ECMO抗凝策略
国际血栓与止血协会(The International Society of Thrombisis and Hemostasis,ISTH)指南[5]推荐,对于重症COVID-19患者,并不推荐采用治疗剂量抗凝。因为低氧加上治疗剂量抗凝,可能会加重脏器出血。所以目前重症COVID-19患者的抗凝仍以预防剂量为主。ELSO指南推荐的活化凝血时间(ACT)180~220 s、保证流量、抗血小板尚未被证实。欧洲和美国的研究发现,当抗凝达到ACT 180~220 s这一目标后,患者出血并发症呈明显升高趋势。所以近年临床对ACT的调整目标偏低,一般采用160~180 s的抗凝目标,以便减少出血并发症。但这也面临一个问题,一旦将ACT目标下调,凝血因子、血小板、纤维蛋白的消耗以及血制品的输注均会明显增多,尤其在重症COVID-19集中暴发期,血制品的需求仍要重点考虑。
ELSO指南和ISTH指南均提到一个问题,即考虑COVID-19患者存在高凝状态,如果加用抗血小板药物,是否会改善抗凝状态,目前仍缺乏相关证据。有小样本研究提示,抗血小板治疗可能会降低患者纤维蛋白原的消耗以及抑制D-二聚体的升高。
尽管研究结果不支持将低分子肝素(LMWH)/普通肝素(UFH)升级到治疗剂量,但除非有禁忌证,否则有明确适应证(如新的或近期的VTE、心房颤动、机械心脏瓣膜)的患者,应提供治疗剂量的LMWH/UFH。
3. COVID-19下对ECMO的思考
对于COVID-19,ECMO究竟辅助到何种程度?对此,MacLaren、Combes、Brodie也针对ECMO上机前、上机中和上机后提出了很多临床关心的问题[6]。ELSO指南提到,COVID-19下的ECMO核心思想是使患者获益,如何获益?首先是患者安全,其次是医护安全,最后是质量控制。此外,个人、设备、场所、系统、伦理也是需要考虑的重要问题。
WHO数据显示,近3年每年都会有COVID-19暴发的小高峰,而且小高峰出现之后也出现死亡率的明显增加。很多患者是在ICU内死亡,当小高峰出现后,ICU的医疗资源一定会出现耗竭。
2021年发表的一项研究纳入了2020年5月1日以前的早期ECMO中心(A1组)、2020年5月2日至12月31日之间早期ECMO中心(A2组),以及2020年5月2日至12月31日后加入的ECMO中心(B组),在5月1日之前,医疗资源尚可,而医疗资源一旦下降,患者死亡率明显增加,且后加入的ECMO中心死亡率更高[7]。这也提示我们,能够开展ECMO的中心,患者预后不一定改善。
2020年1月以前的ELSO数据显示,成人呼吸支持成功率接近69%,出院或能转院的患者达到60%,但COVID-19患者ECMO死亡率居高不下。所以我们在分析ECMO实施的情况下一定要考虑医疗资源耗竭的问题,例如:①在ECMO设备和人员都充足的情况下,可以常规提供服务;②如果ECMO资源已经开始下降,则需要停止体外心肺复苏(ECPR),将更有限的资源分配给VV-ECMO和VA-ECMO患者,而且在年轻且单器官功能衰竭患者中更有优势;③如果ECMO资源进一步下降,则停止VA-ECMO和ECPR,将资源留给年轻且单器官功能衰竭患者;④如果ECMO资源处于耗竭状态,不要提供任何ECMO服务,即使上了ECMO,后期的看护和治疗也达不到预期。
如果是标准的具备ECMO能力的中心(10台以上ECMO设备)或有充足的ECMO资源,可以常规开展ECMO;当资源下降至50%时,就需降低年龄和机械通气时间,而且对于预测VV-ECMO存活率>76%以上者才实施ECMO。如果资源进一步下降,只有25%的能力来提供服务时,需要进一步优化指标[8]。我们最终目的是使更有希望获益的患者得到更好的医疗救治,但这必然涉及伦理问题。所以,医疗机构需要提供专门的ECMO团队来共同解决这些问题。
一篇文章纳入2019年12月1日至2022年4月14日期间42个观察性队列研究中17449例患者,绝大多数患者为50~59岁(以10岁为一个升降),年龄大,男性、合并慢性肺病、肥胖及免疫抑制患者的预后更差。在评估哪些患者能够获益时,高驱动压、症状延续时间长、PaCO2升高、机械通气时间可以作为参考指标[9]。
4. 如何提高ECMO成功率
首先,一定要合理利用ECMO资源。如果在重症高峰期或者集中收治重症患者的情况下,需要整合全院资源合理分配,并且建立ECMO管理团队、规范诊疗行为,合理的医护比(理想的情况是一台ECMO配备一位专业护士进行管理);此外,暴发情况下应集中管理,甚至建立区域级ECMO医疗中心,提高患者救治成功率。
其次,筛选ECMO成功率高的患者,例如年轻、没有基础病、没有明显器官功能衰竭的患者,可能预后较好,但这其中涉及伦理问题,需要专家讨论后谨慎选择。
四、小结
从实战角度出发,COVID-19患者ECMO的实施要从必要性、可行性和风险性三方面考虑。
必要性:在机械通气、俯卧位、肺复张等呼吸支持策略都使用的情况下,患者仍不能改善,就要尽早考虑ECMO,及时改善患者的低氧状态。
可行性:VV-ECMO为主,床旁快速建立,有经验的团队为佳。
风险性:①患者病情是否可逆,在上机之前需与患者家属充分沟通;②抗凝仍有挑战,需权衡出血风险与各种凝血因子消耗之间的利与弊;③重症患者远期预后仍缺乏数据;④在医疗资源耗竭情况下,如何提高重症患者的存活率,根据各个中心的具体情况制订策略。
[1] Yamamoto R, Kaito D, Homma K, et al. Early intubation and decreased in-hospital mortality in patients with coronavirus disease 2019[J]. Crit Care, 2022, 26(1):124.
[2] 中华医学会呼吸病学分会危重症学组,中国医师协会呼吸医师分会危重症医学专家组. 奥密克戎变异株所致重症新型冠状病毒感染临床救治专家推荐意见[J]. 中华结核和呼吸杂志, 2022, 46(2). DOI: 10.3760/cma.j.cn112147-20221230-00994.
[3] Kazi A W, Summer R, Sundaram B, et al. Lung recovery with prolonged ECMO following fibrotic COVID-19 acute respiratory distress syndrome[J]. Am J Med Sci, 2022, S0002-9629(22)00492-X.
[4] Emerson D, Sharifpour M. ECMO in COVID-19: Continued Variable Outcomes[J]. Ann Thorac Surg, 2022, 114(1):75-76.
[5] Schulman S, Sholzberg M, Spyropoulos A C, et al. ISTH guidelines for antithrombotic treatment in COVID-19[J]. J Thromb Haemost, 2022, 20(10):2214-2225.
[6] MacLaren G, Combes A, Brodie D. What's new in ECMO for COVID-19?[J]. Intensive Care Med, 2021, 47(1):107-109.
[7] Barbaro R P, MacLaren G, Boonstra P S, et al. Extracorporeal membrane oxygenation for COVID-19: evolving outcomes from the international Extracorporeal Life Support Organization Registry[J]. Lancet, 2021, 398(10307):1230-1238.
[8] Deitz R L, Thorngren C K, Seese L M, et al. Evolution of extracorporeal membrane oxygenation trigger criteria in COVID-19 a-pqewqlgfdsaMZ respiratory distress syndrome[J]. J Thorac Cardiovasc Surg, 2022, S0022-5223(22)01157-6.

顾思超











