近年来,维持治疗成为卵巢癌慢病管理的主要方法。随着PARP抑制剂在一线维持治疗的探索不断深入,其在初始治疗后延缓甚至遏制卵巢癌复发方面,显示出了前所未有的生存获益,也促使PARP抑制剂快速成为一线维持治疗的常用方案。对于BRCA阴性,初始肿瘤细胞减灭术(PDS)不满意,辅助化疗达部分缓解(PR)的Ⅳ期卵巢癌患者何时可启动PARP抑制剂的一线维持治疗,PARP抑制剂长期维持治疗是否可遏制肿瘤复发、转移成为人们关注的问题,本病例分享PARP抑制剂在初治晚期卵巢癌患者延缓复发方面的应用经验。

伍成荣 主治医师
贵州医科大学附属医院
2009年毕业于遵义医科大学妇产科学专业,从事妇产科专业10年,现就读于贵州医科大学妇产科,硕士研究生 三年级,参与科研课题多项,发表SCI论文一篇。
01
病例回顾
基本资料
患者,女性,58岁。婚育史:已婚,G2P1,顺产、人流各一次。月经史:初潮14岁,4-5天/25-30天,末次月经(LMP):2020-2-22。既往史:“双侧颈部淋巴结脓肿”脓肿清除术、“宫颈管息肉”摘除术、高血压病史。家族恶性肿瘤史:母亲“肺癌”、父亲“食管癌”,均已故。
病史特点:
患者于2020年3月自行扪及腹部包块,无腹痛、腹胀、异常阴道流血、流液等。
体格检查无异常。妇科检查:阴道后穹窿饱满,宫颈II°糜烂样改变,子宫稍大,形态不规则,边界不清,活动度可,后方偏右侧可扪及一大小约10 cm×10 cm×9 cm包块,质硬,固定,无压痛。移动性浊音(-)。
MRI:肝脏后缘及下缘、升结肠周围、腹膜后主动脉周围多发结节状、团片状影,考虑转移灶;盆腔内囊实性占位,大小约101 mm×75 mm×124 mm考虑来源于右侧,卵巢恶性病变:囊腺癌,右侧盆腔肿大淋巴结转移,腹膜种植转移,盆腔积液。
胸部CT示:左肺上叶纤维化病灶。
PET-CT:盆腔内见一不规则巨大囊实性病变,以囊性为主,其内见分隔,较大横截面约10.0 cm×9.6 cm,子宫及膀胱受压,与邻近盆腔腹膜分界不清,病变实性部分、囊性及分隔可见不均匀FDG摄取增高至浓聚,最大SUV为17.3;左锁骨上区、纵隔6区,右侧膈区、右侧膈脚、腹腔、腹膜后及双侧髂血管走行区见多发淋巴结影,部分明显肿大,较大者约2.9 cm×2.2 cm,伴FDG摄取增高,最大SUV为12.7;子宫体积增大,宫颈增粗,未见FDG摄取增高;子宫周围见液体密度影。咽淋巴环区见对称性FDG摄取;右下肺见一小结节状增高密度影;双乳腺体FDG摄取轻度增高,最大SUV 2.8;左肾实质内见小囊状低密度影,直径约0.2 cm;右肾实质内见一小结节状脂肪密度影,直径0.3 cm,伴FDG分布稀疏至缺损。其余组织器官无明显异常。
肿瘤标志物:CA125 666.9 U/ml,HE4 777.9 pmol/L,POMAH 97.32%,POMAQ 98.59%。
初步诊断:卵巢恶性肿瘤Ⅳ期,盆腹腔肿瘤转移,原发性高血压。
治疗经过
✔第一阶段:初始细胞减灭术+术后化疗
2020-3-19行PDS。术中见腹水:淡血性,约200 ml;肝、胆、脾、肾:光滑,未触及明显结节,左侧盆腹膜表面见一肿瘤组织,约0.2 cm,鱼肉样;大网膜:表面见三个实性灰白色肿瘤附着,直径分别为2 cm、3 cm、3 cm,质硬,灰白色;淋巴结(盆腔、腹主动脉旁):髂总以上淋巴结呈片状增厚,质硬,如盔甲样包绕在动脉和静脉周围,与血管致密粘连,盆腔淋巴结未扪及明显增大。膀胱腹膜返折右侧可见一0.5 cm 肿瘤突起,呈鱼肉样。盆腔:子宫:略大,右侧肌瘤样突起,大小约1 cm×1 cm×1.5 cm;双附件:右附件与盲肠致密粘连,右卵巢增大,约10 cm×10 cm×9 cm,质硬,与子宫后壁致密粘连,直肠子宫陷凹及直肠表面可见多枚0.5-2.5 cm实性、灰白色肿瘤堆积,右侧骶韧带增粗,表面见肿瘤病灶,约0.3-2 cm,双侧输卵管及左侧卵巢外观无明显异常;部分乙状结肠与左侧盆壁粘连,未见明显异常;小肠、升结肠、横结肠、降结肠、回肠均未见明显异常。手术切除范围:双附件及子宫、大网膜、肉眼可见癌组织、腹主动脉旁淋巴结清扫至接近II水平,其以上区域仍有大块增厚淋巴组织。
术后病理:右侧附件:右附件浆液性腺癌(高级别)。累及子宫颈外壁,深度达肌层,阴道残端见癌累及,大网膜脂肪组织内癌组织浸润并癌结节形成,腹主动脉旁淋巴结12枚均见癌转移,腹膜结节纤维组织内癌组织浸润并癌结节形成。免疫组化:CK(+),EMA(+),Vim(-),P53(-),P16(+),PAX8(+),WT1(+),ER(+部分),PR(auto-),CD3(-),CD20(-),Ki-67(+30-40%),支持高级别浆液性癌。
术后基因检测:BRCA无致病突变,未测HR(图1)。
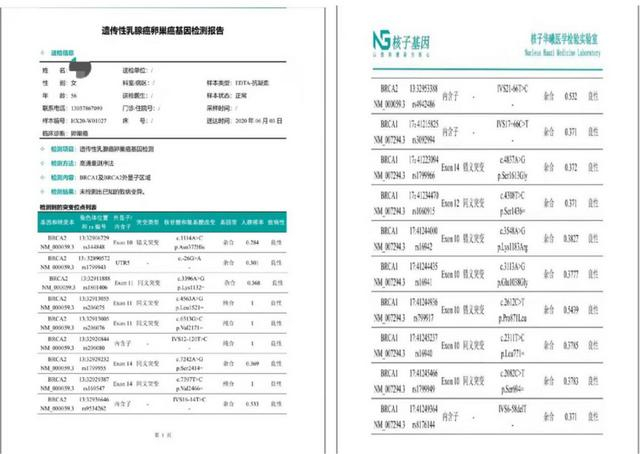
图1.患者基因检测报告
术后诊断:1、双侧卵巢高级别浆液性癌Ⅳ期;2、肠粘连;3、原发性高血压。
术后行紫杉醇注射液+顺铂方案化疗6个周期(2020-3-25至2020-7-14)。化疗期间主要身体指标变化:
1. 肿瘤标志物:CA125、绝经前罗马指数(pre-ROMA)、绝经后罗马指数(post-ROMA)降至正常(图2、图3、图4),HE4在正常范围内进行性下降(图5);
2. 盆腔超声检查:2020-5-7腹部B超发现平脐偏右腹腔内低回声团块,化疗期间该团块变化(图6):
第二次化疗后团块大小61mm×22 mm,边界欠清,未见血流;
第三次化疗后团块大小48mm×20 mm;
第四次化疗后团块大小35mm×14 mm;
第五次化疗后团块大小33 mm×16 mm×12 mm。
3. 手术及化疗后RECIST评估达PR。
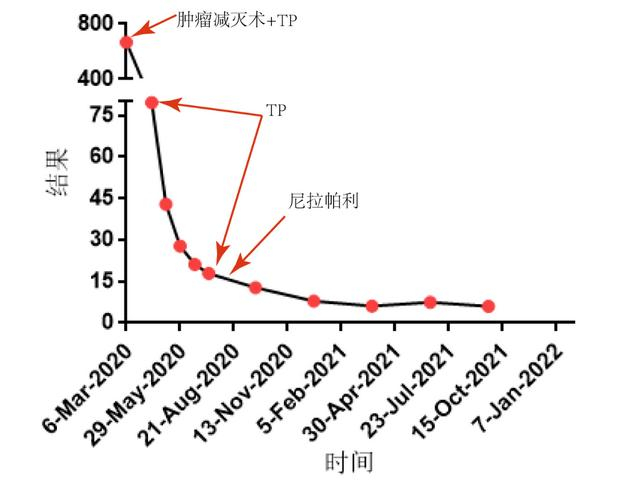
图2.患者CA125水平变化情况
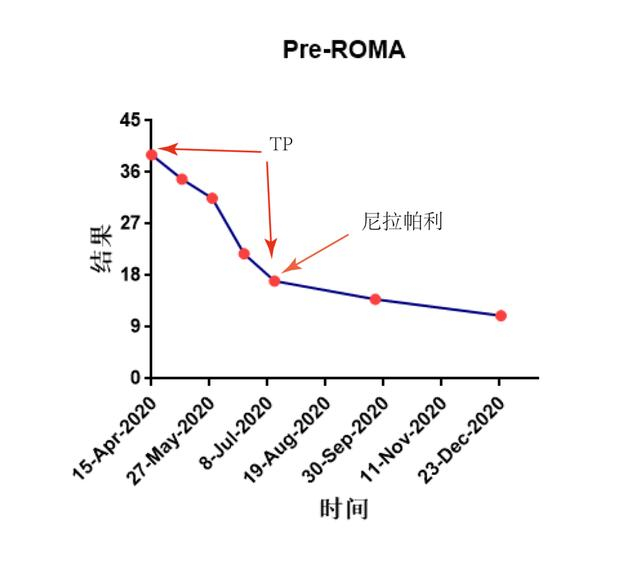
图3.患者pre-ROMA变化情况
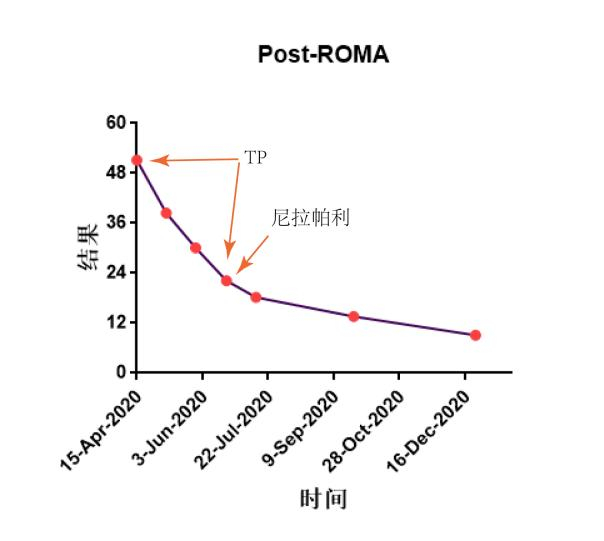
图4.患者post-ROMA变化情况
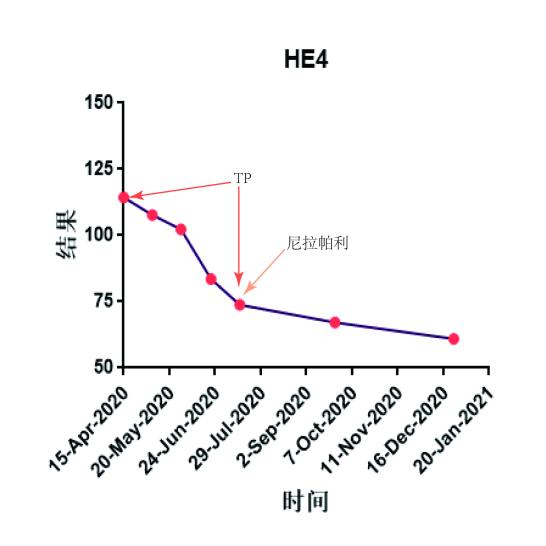
图5.患者HE4水平变化情况
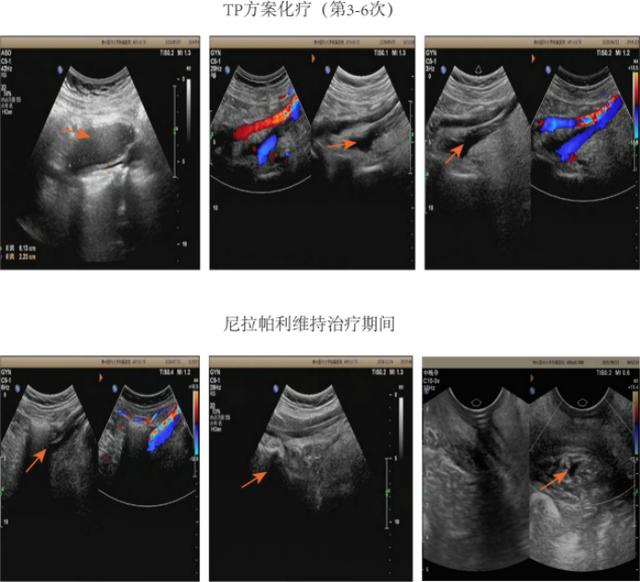
图6.患者超声影像
✔第二阶段:PARP抑制剂维持治疗
化疗结束一月(2020-8-14)开始口服尼拉帕利,剂量:200 mg/天。服药期间主要的不良反应:恶心、睡眠差,偶有口腔溃疡;随着治疗时间延长症状消失。
身体指标变化:
白细胞、红细胞、血小板、肝肾功均正常;
肿瘤标志物:治疗期间CA125、HE4、Pre-ROMA、Post-ROMA仍在正常范围内呈下降趋势(图1-4)。
影像学检查:
2020-12-25腹部CT,示腹主动脉以上淋巴结肿大。
2021-9-25腹部CT,示腹主动脉以上淋巴结肿大较前明显改善(图7)。
2020年7月腹部超声检查:原盆腔病灶大小约33 mm×16 mm×12 mm。
2021年9月腹部超声检查:原病灶大小13 mm×9 mm(图6)。
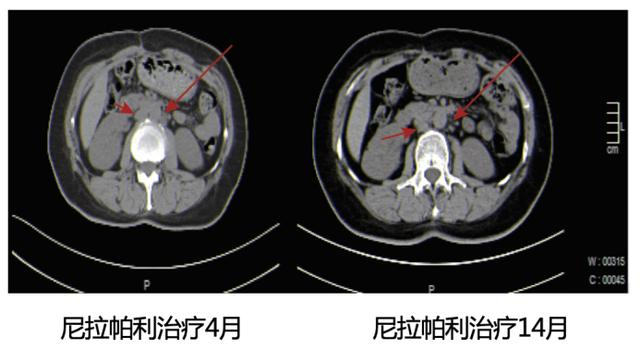
图7. 腹部CT影像
病例总结
患者自行扪及腹部包块,无不适,外院B超、MRI发现盆腔占位,CA125 666.9 U/ml;HE4 777.9 pmol/L,POMAH 97.32%;POMAQ 98.59%。遂来院就诊,综合各项检验、检查结果提示卵巢恶性肿瘤并盆腹腔转移。治疗先行PDS,术后诊断:双卵巢高级别浆液性癌Ⅳ期。术后行紫杉醇+顺铂方案化疗6个周期,CA125降至正常,RECIST评估达PR,BRCA阴性。2020年8月起口服尼拉帕利200 mg qd维持治疗。CA125、HE4、Pre-ROMA、Post-ROMA在正常范围内波动。复查CT,2021-9-25示腹主动脉以上淋巴结肿大较前明显改善。复查彩超,示盆腔包块病灶逐渐缩小,2021-9-23为13 mm×9 mm。
03
专家点评

蔡华蕾
贵州医科大学附属医院
副主任医师,副教授,硕士研究生导师,国家二级心理咨询师。长期从事妇产科临床、教学、科研工作,擅长妇科开腹手术,腹腔镜、宫腔镜手术和性激素治疗。

专家点评
卵巢癌病死率占据妇科恶性肿瘤首位。卵巢癌的治疗原则强调以手术、化疗及维持治疗为一体的综合治疗。PDS是中晚期卵巢癌治疗的重要组成部分,美国国立综合癌症网络(NCCN)指南推荐:适合手术或满意减瘤的患者,可以选择PDS
[1]
。术后充分化疗,可防止肿瘤复发和转移。紫杉醇与顺铂联合化疗方案,是卵巢上皮性癌的首选联合化疗方案之一
[2]
。结合本例患者,卵巢恶性肿瘤并盆腹腔转移,入院经充分评估,PDS+术后紫杉醇与顺铂联合治疗,评估治疗后达PR,且BRCA阴性。那么,对于该例患者,PDS后残留较多病灶,术后以铂为基础的初始治疗结束后,又该如何维持治疗呢?多项临床研究已证实,对于新诊断的Ⅱ~Ⅳ期高级别浆液性卵巢癌患者,在手术和以铂类为基础的治疗后达到完全缓解(CR)或PR,给予PARP抑制剂维持治疗可带来临床获益
[1]
。PRIMA研究是第一个无论BRCA突变和HRD状态,将PARP抑制剂单药作为卵巢癌一线维持治疗的III期临床试验
[3]
,研究结果显示,在为期36个月的一线维持治疗后,在总人群中尼拉帕利组较安慰剂组疾病进展或死亡风险降低38%[中位无进展生存期(PFS)分别为13.8个月和8.2个月,HR 0.62,95% CI 0.50~0.75,P<0.001];同时,在总生存期(OS)的期中分析中,尼拉帕利组较安慰剂组也显示出了较高的总生存获益趋势(HR 0.70,95% CI 0.44~1.11);且尼拉帕利组安全性较安慰剂组无显著差异。诸如NCCN等指南已将尼拉帕利推荐用于初始化疗未使用贝伐珠单抗且BRCA阴性患者的一线维持治疗
[4]
。我们在跟患者充分沟通后,患者选择了尼拉帕利治疗,经过17个月的治疗后,我们惊奇地见到了患者残留病灶在缩小,并且没有新增病灶,尼拉帕利维持治疗期间,监测血常规、肝肾功等指标无明显异常,肿瘤标志物CA125、HE4、Pre-ROMA、Post-ROMA保持在正常水平,原有高血压病没有加重。生活质量良好,患者的生活已回到正常状态。
回顾分析该例患者的诊治经过,双侧卵巢高级别浆液性癌Ⅳ期伴原发性高血压,PDS+以铂为基础的初始化疗后达PR,肿瘤基因检查BRCA阴性。尽管手术已不能将病灶切净,选择敏感化疗药物是控制残留肿瘤的第一步,化疗后根据肿瘤的基因检测选择合适的PARP抑制剂,适时上药,可能是这例患者取得较好疗效的关键,但患者取得良好效果的确切原因并不清楚,还需要深入的研究。该患者的治疗经历为残留较多病灶的晚期患者带来了希望。PDS、紫杉醇+顺铂化疗以及PARP抑制剂维持治疗的一体化治疗策略,延缓了该例患者的恶性肿瘤进展;并通过充分的患者教育、定期随访、严密的血压监测,实现了卵巢癌的全程管理模式,最终使患者获得了更好的临床预后。希望本例BRCA阴性的Ⅳ期卵巢癌患者的全程管理模式,能够为卵巢癌的慢病管理带来新的思考,从而为更广泛人群带来更好的生存获益。
参考文献
[1] 卢淮武,许妙纯,张钰豪,等.《2021 NCCN卵巢癌包括输卵管癌及原发性腹膜癌临床实践指南(第1版)》解读[J].中国实用妇科与产科杂志,2021,37(4):457-466.
[2] 中国抗癌协会妇科肿瘤专业委员会.中国卵巢上皮性癌维持治疗指南(2021年版)[J].中国实用妇科与产科杂志.2021,37(6):640-648.
[3] Gonzalez-Martin A,Pothuri B,Vergote I,et al.Niraparib in patients with newly diagnosed advanced ovarian cancer.N Engl J Med.2019;381(25):2391–2402.
[4] NCCN Guidelines®. Ovarian Cancer Including Fallopian Tube Cancer and Primary Peritoneal Cancer. Version 1.2020. available at www.nccn.org.











