方案A:利用CellVue®染料标记细胞
CellVue®是一种亲脂性染料,可以用来标记细胞膜,以识别和跟踪被标记的细胞。细胞标记过程快速而稳定,能够与荧光标记的抗体和其他细胞功能标记物并用,用于流式细胞分析和荧光显微镜检查。
一般注意事项
– Mini CellVue® 试剂盒中含有一瓶染料原液(1mM的乙醇溶液)和一瓶标记介质(稀释液 C);Midi CellVue C ® 试剂盒内含两瓶染料原液(稀释液 1mM的乙醇溶液)和六瓶标记介质(稀释液 C);
– 所有过程均在室温下进行。标记过程中不应使用含有叠氮化物或其他代谢抑制剂的试剂。
实验步骤
注:该方案经过体内或体外细胞标记的测试。因为标记有赖于细胞膜结合染料,因此如果染料浓度过高,或者标记时间过长,都会破坏细胞膜完整性,细胞状态也会较差。应该在单克隆抗体染色之前,利用CELLVUE@染料标记。研究者应该根据实验需要摸索标记的条件和浓度,确保染料发挥最佳性能。
1.利用不含血清的培养基洗涤细胞,去除会干扰细胞标记的血清蛋白质和脂质。
2.小心地倒掉上清液,留下不超过25uL的培养基。
3.用稀释液C重悬细胞,使浓度达到2×107细胞/mL, 禁止涡旋。吹打几次,确保形成单细胞悬液。
4. 标记前用稀释液C制备2X染料工作液。如果染料的终浓度是2uM,需将4ul 1mM染色原液加到1ml稀释液C中,制备4uM染色浓液。为确保标记均匀,不能将染料原液直接加入单细胞悬液中。
5. 快速将1ml细胞加入到1mL2x染色工作液内,吹打混匀样本确保标记均匀。最终细胞浓度应该约为1×107细胞/mL,最终染料溶度应该为2uM。
6. 孵育2-5分钟,孵育期间需混匀几次。孵育时间越长标记越明亮,但是应避免过久对细胞活性产生影响。
7.加入等量的血清孵育1分钟终止标记。
8.离心细胞并弃上清。
9. 使用完全培养基洗涤细胞三次(不用稀释液C)。为降低残留染料的干扰,将细胞转移到新试管中。
10.根据需要进行细胞计数、培养或转移。
方案B :利用细胞增殖染料(CPD)eFluor® 450
细胞增殖染料(CPD)eFuor® 670,CPD eFluor@ 450,和5-(和6)羧基荧光素二醋酸盐琥珀酰亚胺脂(CFSE)是可以监测单细胞分裂的荧光染料。该染料可以在体内跟踪未分裂的细胞数周。该染料与细胞蛋白质形成共价反应。随着细胞分裂,该染料会均分到子代细胞中,荧光强度减为原来的一半。根据使用的染料,我们可以继续观察6-8代细胞。增殖染料标记的细胞可以被含甲醛的固定剂和皂角素的破膜液固定并破膜,例如Foxp3/转录因子染色缓冲液试剂盒(货号 00-5523)或细胞内固定&破膜液试剂盒(货号 88-8824),然后进行细胞内抗原的分析。
材料
– CPD eFluor®450 (货号 65-0842)
– 无菌1X PBS
– 二甲基亚砜(DMSO),无水
– 培养基(含≥10%血清)
实验步骤
1.一管CPD eFluor@ 450中加入126 mL无水DMSO溶解形成10mM染料原液。
注:溶解后,应避光存放在-20℃的条件下,干燥保存。建议在6个月内使用该染料,避免反复冻融。
2.制备需要标记的单细胞悬液。
3.利用PBS洗涤细胞两次,清除所有血清。
4. 在PBS(预热至室温)中重悬细胞,使浓度达到最终所需的两倍。例如,最终浓度为10×106细胞/mL, 则重悬细胞浓度为20×106细胞/mL。
注:最终细胞浓度不应超过10X106细胞/mL。如果标记细胞总数不超过5X106细胞/mL,则使用的PBS不应少于0.5mL。
5.PBS(预热至室温)制备20uM的CPD eFluor@ 450。按照1:1的比例混合CPD工作液和第6步制备的2X细胞悬液。
注:建议将10uM作为标记细胞的起始点;但是,强烈建议根据测试结果确定最佳浓度。
6.涡旋2X细胞悬液,并加入等量的第5步制备的染料溶液。
7.室温避光孵育20分钟。
8.加入4-5体积预冷的完全培养基(含>10%血清)终止标记,并在冰上孵育5分钟。
9.用完全培养基洗涤细胞三次。
10.根据需要进行细胞培养和转移。
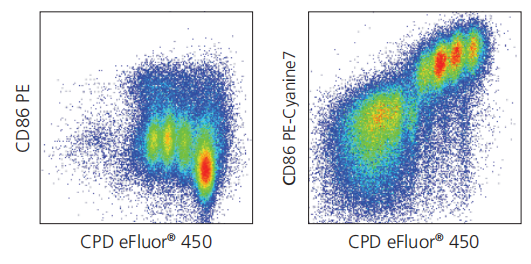
细胞活化和增殖
左图: 利用CPD eFluor®450标记人PBMC细胞,并与刀豆蛋白A(ConA)溶液(500X)(货号 00-4978)一起培养3天。使用抗人CD86 PE(货号 12-0869)和细胞活性染料FVD eFluor®660(货号65-0864)染色。设门淋巴细胞及活细胞后进行分析。右图:利用CPDefuor®450标记小鼠脾细胞,并与刀豆蛋白A(ConA)溶液(500X)(货号00-4978)一起培养3天。使用抗小鼠CD86 PE-Cyanine7(货号25-0862)和细胞活性染料FVD eFluor®660(货号 65-0864)染色。设门淋巴细胞及活细胞后进行分析。
方案C:羧基荧光素二醋酸盐琥珀酰亚胺脂(CFSE)
材料
– CFSE(货号 65-0850)
– 无菌1X PBS
– 甲基亚砜(DMSO),无水完全培养基(含≥10%血清)
实验步骤
1.90 μL无水DMSO溶解一瓶DMSO成10mM浓缩原液。
注:溶解之后,应避光存放在-20°℃的条件下,干燥保存。建议在6个月内使用该重组染料,避免反复冻融。
2.制备需要标记的单细胞悬液。
3.利用PBS洗涤细胞两次,清除所有血清。
4.使用PBS(预热至室温)重悬5-10×105细胞/mL。
5.加入CFSE至所需浓度(例如:最终浓度为1uM时,每毫升细胞加入0.2uL5mM原液)。
6.立即混匀,并在室温避光孵育10分钟。
7.加入4-5体积预冷的完全培养基终止标记,并在冰上孵育5分钟。
8.用完全培养基洗涤细胞三次。
9.根据需要进行细胞培养和转移。
注:CFSE的浓度、孵育时间和温度可达到理想的染色强度。但是荧光信号过强会导致补偿难以调整,也可能会干扰细胞的功能。因此,强烈建议根据测试结果确定最佳浓度。
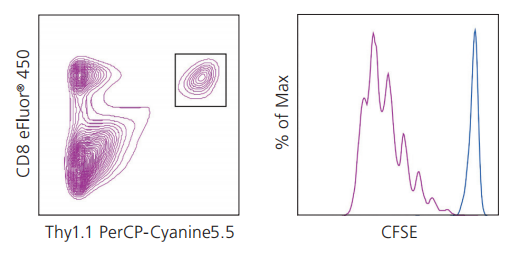
细胞增殖对OVA处理的反应
利用1 μM CFSE标记OT-I小鼠的淋巴结细胞,打入C57BI/6小鼠体内。三天以后,利用抗小鼠/大鼠CD90.1(Thy1.1)PerCP-cyanine5.5(货号 45-0900)和抗小鼠 CD8a eFluor® 450(货号 48-0081)染色小鼠脾细胞,为OT-I细胞设门(左图)。分析OT-I门内(CD8+Thy1.1+)细胞的分裂(右图),OVA免疫小鼠测定出离散的CFSE峰值(紫色直方图),而PBS免疫小鼠的未分化细胞为单独明亮的CFSE峰值(蓝色直方图)。