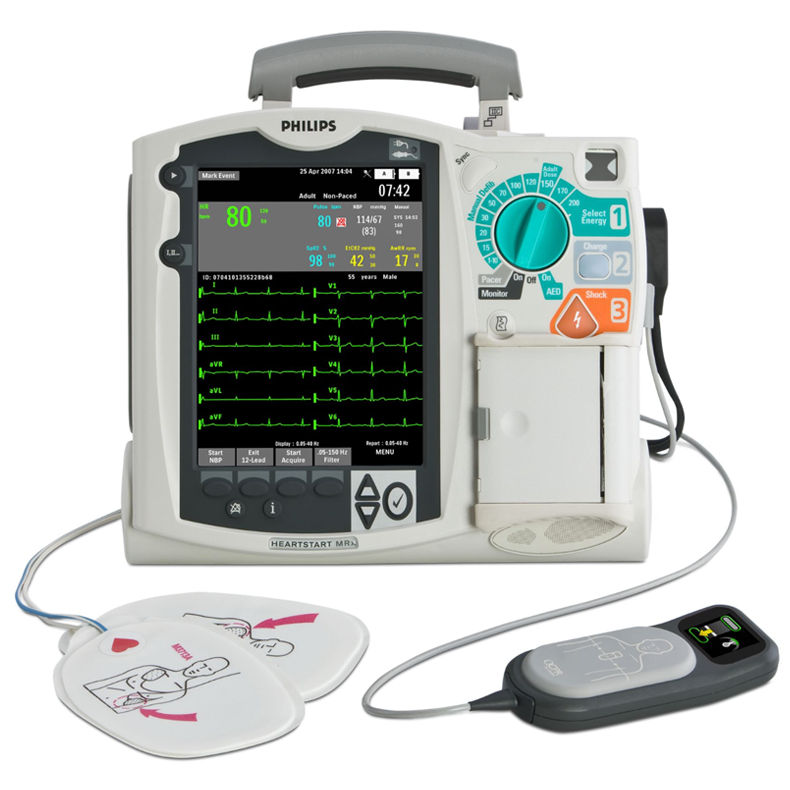
一、引言
在此,我们提出了一种用于集成光遗传学和电生理学的透明植入式电极阵列的制造方案。我们描述了使用导电聚合物聚(3,4-乙烯二氧噻吩):聚(苯乙烯磺酸盐)制造微电极的步骤。然后,我们详细介绍了分析电极性能和记录转基因小鼠光诱发神经活动的程序。该方案利用光刻法而不是传统的电沉积。
二、开始之前
通过电生理记录评估复杂脑神经活动的方法已成为神经科学家和脑工程师识别人类行为机制的基石。此外,为了减轻患有各种神经系统疾病(帕金森病、阿尔茨海默病或抑郁症等)的患者的负担,电生理学在分析来自大脑的电信号以找到适当的治疗方法方面发挥着重要作用。与电生理学方法无关,用光控制神经活动的光遗传学也作为一种神经元特异性调制方法而受到关注。光遗传学通过基因改造特定的目标神经元,实现了比电刺激具有更高选择性的神经活动改变。
因此,电生理学和光遗传学的结合在实时监测来自大脑的电信号和神经元特异性调制方面带来了显著的协同效应。同时用电生理学记录单个神经元和轴突投射是否受到预定频率的光调制,降低了复杂神经系统疾病电路分析的难度,而这在以前是不可能的。
然而,电生理学和光遗传学融合时会出现严重的问题-1.光电伪影,2.有限的光传输。神经电极引起的光电伪影是指当高于一定能量水平的光施加到金属电极表面时,激发自由电荷产生的小电压信号。当此电压信号与来自神经活动的微小电生理电位结合时,会导致神经信号污染。此外,不透明的金属电极会吸收大部分用于神经调节的光,从而阻止光遗传学所需的足够能量到达脑组织。这种有限的光传输不利于电生理学和光遗传学的融合,因为神经活动不会在光刺激阈值下被激活。
透明的可植入电极阵列不会吸收但会传输大部分用于刺激的光,因此同时进行电生理学和光遗传学刺激几乎没有问题。通常,导电氧化物(例如氧化铟锡)具有高光学透明度和电导率。然而,由于机械脆性,限制了它难以应用于柔性生物植入装置。利用石墨烯或碳纳米管等二维材料的电极阵列以其光学透明而灵活的形式成为电生理学和光遗传学融合的重要桥梁。然而,由于活性电极层在功能化柔性基板上的转移过程而导致的电极制造困难一直是碳基材料应用的主要挑战。PEDOT:PSS 是一种导电聚合物,具有高透光率和优异的机械性能,并且由于分子结构的改性,可以预期具有高电导率。
在这里,我们介绍了一种使用 PEDOT:PSS 制造植入式透明电极的方案。与现有的在传统金属上用电镀沉积 PEDOT:PSS 的方法不同,该方案引入了使用超声波剥离对 PEDOT:PSS 进行图案化旋涂。由单层 PEDOT:PSS 构成的透明电极阵列无需添加金属,在整合电生理学和光遗传学时不存在两个问题 – 光电伪影和有限的光传输。我们的方案详细介绍了如何使用蓝色激光控制转基因小鼠的神经信号,同时进行高保真神经记录,且光诱导伪影可忽略不计。通过介绍透明电极制造方法和无伪影电生理学与光遗传学,本文展示了基于导电聚合物的神经植入物作为以前未发现的神经回路分析工具的潜力。
三、机构许可(如适用)
韩国首尔的韩国科学技术研究院 (KIST) 批准了所有与动物相关的程序,这些程序均按照 KIST 动物护理和使用指南中概述的道德准则进行。
3.1 基底制备
时间:4 小时
1. 制备贴在载玻片临时基底上的 PET(聚对苯二甲酸乙二醇酯)薄膜基底。
a. 制备载玻片(75 毫米 × 25 毫米 × 1 毫米)。然后,另外制备聚二甲基硅氧烷 (PDMS) 溶液。
b. 在方形聚苯乙烯称量盘中装入 32 克 PDMS 基底溶液后,添加 2 克固化剂并充分混合,使基底和固化溶液的比例为 16:1。
c. 将装有混合 PDMS 溶液的盘子放入真空干燥器后,对腔室进行抽真空,直到 PDMS 中的气泡完全消失(图 1A)。
重要提示:如果在 PDMS 中的气泡未消除的情况下使用混合溶液,则稍后固化涂层 PDMS 时可能会因气泡过多而导致基底产量降低。建议将干燥器中的真空度保持至少 1 小时。
图 1. 用于制造具有电生理记录的传统金 (Au) 电极和透明 PEDOT:PSS MEA 的设备。(富临塑胶供应PEDOT:PSS MEA 设备)
(A) 干燥器 (B) 旋涂机 (C) 紫外线 (UV) 对准器 (D) 反应离子蚀刻机 (RIE) (E) 超声波仪 (F) 分光光度计 (G) 恒电位仪 (H) INTAN 仪 (I) 热蒸发器。
d. 将载玻片固定在旋涂机卡盘上并保持真空后,将准备好的 PDMS 溶液完全倒在玻璃上。旋涂机如图 1B 所示。
e. 将倒出的 PDMS 以 2000 rpm 的速度旋涂在玻璃上 50 秒。
f. 为了逐渐固化 PDMS,将涂覆的临时玻璃基板在 70℃ 下加热 30 分钟,然后在 110℃ 下加热 30 分钟。
g.将厚度为 25 μm 的 PET 薄膜基板切割成合适的样品尺寸(3 cm × 2 cm),并将其压在完全硬化的玻璃上的 PDMS 上。
关键资源表
3.2 分步方法详细信息
3.2.1 透明 PEDOT:PSS 神经电极的制造
时间:4 小时
在这项工作中,我们介绍了使用导电聚合物聚(3,4-乙烯二氧噻吩):聚(苯乙烯磺酸盐)(PEDOT:PSS)使用光刻剥离法进行电极阵列微图案化的过程(图 2A)。由于 PEDOT:PSS 的固有酸性,研究人员在使用光刻过程中所需的显影剂时必须小心与溶液的直接接触。为了获得更高的图案化分辨率,协议中还详细介绍了在剥离过程中使用超声波仪器去除残留光刻胶材料的过程。
1.在 PET 基板上微图案化电极阵列。
a. 按照丙酮、异丙醇 (IPA) 和去离子水 (DI) 的顺序清洁层压 PET 薄膜基板(图 2B)。
b. 以 2000 rpm 的速度在 PET 基板上旋涂 AZ 5214 光刻胶 50 秒(图 2C)。
c. 用 110℃ 的热板烘烤样品 2 分钟(图 2D)。
d. 将样品放在光对准器上后,用电极形微图案光掩模覆盖样品。
e. 将样品暴露在紫外线 (UV) 下(强度:14.3 W/s)8 秒(图 1C 和 2E)。
严重:即使只有几个小颗粒进入涂有光掩模和光刻胶的样品,也会对微电极制造造成严重问题。由于电极外部连接的线宽约为50μm,因此需要提前防止此连接因外部异物而断开。
f.将部分暴露在紫外线下的涂有光刻胶的样品放在120℃的加热板上加热2分30秒(图2F)。
g.样品充分冷却后,将其放回光对准器上,并在没有光掩模的情况下将所有部分暴露在紫外线(强度:14mW)下14秒(图2G)。
h.在培养皿中倒入适量的显影剂(AZ 300 MIF)后,将样品浸入其中2分30秒(图2H)。
关键:如果对样品进行显影的时间太长,已被加热板完全硬化的光刻胶部分(应该是抗蚀剂聚合物的部分)也会被显影剂消失。在显影液中浸泡的时间最多不得超过 4 分钟。
i. 将样品从显影液中取出,用 DI 清洗 20 秒后,用氮气吹枪去除残留的水。
2. 在 PET 薄膜基板上旋涂并剥离 PEDOT:PSS。
a. 将微图案化的 PET 薄膜基板放入反应离子蚀刻 (RIE) 室中。
b. 在表面进行氧等离子体处理 (20 sccm、100 W、30 秒)(图 1D 和 2I)。
关键:如果不进行氧等离子体处理,PEDOT:PSS 将不会旋涂在 PET 薄膜疏水表面上的电极图案上。在溶液状态下涂覆 PEDOT:PSS 时,必须先进行此过程以形成具有均匀厚度的电极阵列层。
c.将亲水表面处理过的样品固定在旋涂机卡盘上,并在表面涂抹 PEDOT:PSS 溶液(Clevios PH 1000,比例 1:2.5)(1500 rpm,40 s)(图 2J)。
d.将 PEODT:PSS 涂层样品在 110℃ 的加热板上交联 10 分钟(图 2K)。
e.将样品浸入丙酮中 15 分钟(图 2L)。
关键:必须用丙酮牺牲的光刻胶层位于旋涂的 PEDOT:PSS 层下方。因此,在使用超声波进行剥离工艺之前,必须让丙酮溶液渗透光刻胶至少 15 分钟。
f.将装有样品和丙酮的烧杯放入超声波处理室,在操作超声波处理室的同时适度摇晃 20 秒(图 1E 和 2M)。
g.将样品从烧杯中取出,用 IPA 彻底清洗 30 秒。
h.将样品在 110℃ 的加热板上固化 10 分钟。
3.对 PEDOT:PSS 微电极阵列 (MEA) 进行后处理。
a.准备乙二醇 (EG)。
b.将适量的 EG 倒入培养皿后,将样品浸泡 30 分钟(图 2N)。
c.取出样品,用 IPA 清洗 1 分钟。
关键:EG 溶液使处理过的表面变得光滑,并且具有即使经过 IPA 清洗后残留物也不易消失的特性。如果残留有 EG,则在封装后过程中很难形成合适的环氧树脂图案以确定记录位置,因此必须留出足够的 EG 清洁时间。
d. 将样品放在 110℃ 的加热板上加热。
4. 封装 PEDOT:PSS-EG MEA,但记录位置除外。
a. 用 IPA 重新清洁完全固化的 PEDOT:PSS-EG MEA 20 秒后,用氮气去除残留水分。
b. 将样品固定在旋涂机卡盘上后,用 UV 固化环氧树脂 (SU 8–2000.5) (3000 rpm,40 秒) 旋涂样品(图 2O)。
c. 将样品放在 100℃ 的加热板上 2 分钟。
d.将样品放在光对准器上后,用样品上的记录位置图案覆盖光掩模,并将其暴露在紫外线下 4 秒(图 2P)。
e.将样品再次放在 100℃ 的热板上,加热 2 分钟,交联 30 秒。
关键:UV 固化环氧树脂的硬烘烤过程比软烘烤重要得多。在软烘烤(2 分钟)的情况下,超过固化时间不会直接影响设备的完成。但是,如果根本没有进行硬烘烤过程或没有遵循指定的固化时间,则无法对样品进行图案化。
f.将样品浸入 UV 固化环氧树脂显影剂中 1 分钟(图 2Q)。
g.取出样品并用 IPA 清洗 40 秒。
关键:用丙酮或去离子水清洗未完全硬化的 UV 固化环氧树脂可能会对完成的电极图案产生负面影响,因此务必用 IPA 彻底清洗样品。
h.将样品再次放在 120℃ 的热板上 1 小时以硬固化。
5.切割完成的 MEA 并将其连接到外部神经记录设备。
a.用显微镜检查完成的 MEA 的接口时,使用刀片切割设备。
b.准备各向异性导电膜 (ACF),将外部记录设备中的印刷电路板 (PCB) 与样品连接。
c.根据设备的通道数切割 ACF 后,将其与设备的互连线接触,同时进行粘合,并在低温下熨烫。
d.根据切割面小心地将完成的样品从带有玻璃基板的 PDMS 上分层。
图 2. 透明 PEDOT:PSS MEA 的详细制造过程
(A) 透明 PEDOT:PSS MEA 的逐步制造过程。(B) 基板准备 (C) AZ 5214 旋涂 (D) 软烘烤 (110℃) (E) 紫外线曝光 (F) 硬烘烤 (120℃) (G) 紫外线整体曝光 (H) 显影 (AZ5214) (I) O2 等离子处理 (J) PEDOT:PSS 旋涂 (K) PEDOT:PSS 交联 (L) 丙酮浸泡 (M) 超声波剥离 (N) 乙二醇处理 (O) SU8 旋涂 (P) 紫外线曝光 (Q) 显影 (SU8)。
3.3 透明电极阵列的光学、电化学、机械性能测量
时间:8 小时
此过程是为了确保所制备的电极在进入体内实验之前具有足够的神经记录可行性。通过此询问,分析了电极阵列的光学透明度、电化学性能和机械性能,并确定它们在体内环境中是否稳定。与传统的 Au 电极阵列不同,我们的透明 PEDOT:PSS MEA 具有优异的光学透明度,可与石墨烯相媲美(图 3A)。在电化学阻抗的情况下,我们的电极阵列在 16 个通道的 1 kHz 频带中显示 55 ± 10 kΩ,并且证实这些电性能即使在多次电极弯曲后也不会发生变化(图 3B 和 3C)。此外,此过程检查了透明 PEDOT:PSS MEA 与培养 6 天的皮质神经元的生物相容性。结果,与未经任何处理的玻璃一样,在电极上培养的皮质神经元也仅显示出可忽略不计的细胞死亡(图 3D 和 3E)。
6. 测量 PET 基板上 PEDOT:PSS-EG 薄膜的光学透明度。
a. 将 PDMS 涂层载玻片插入紫外可见分光光度计并扫描样品(参考透射率,旋转速度:2000 nm/min)紫外可见分光光度计如图 1F 所示。
b. 在紫外至可见波长范围内重新测量 PET 基板上透明的 PEDOT:PSS 薄膜。
7. 测量 PET 基板上 PEDOT:PSS-EG MEA 的电化学阻抗谱 (EIS)。
a.在小方盘中准备磷酸盐缓冲溶液(PBS)(Sigma Aldrich,1 L 去离子水中含有 0.01 M PBS)(pH 7.4,36℃)。
b.准备参比电极(Ag/AgCl)、对电极(铂电极)和工作电极(透明 PEDOT:PSS-EG MEAs)。
c.设置阻抗测量仪器(Gamry ref. 600+ 恒电位仪),并将连接三个电极的电缆连接到该系统。Gamry Reference 如图 1G 所示。
d.测量 MEA 的电化学阻抗和相位,频率范围为 1 Hz 至 100 kHz。
关键:测量电化学阻抗时,为了获得准确的数据,请选择低噪声模式,而不是数据采集速度快的模式。
8.根据弯曲次数测量透明PEDOT:PSS-EG MEA的电化学阻抗。
a.在小方盘中准备玻璃棒(直径:0.5 mm)和PBS溶液。
b.以与EIS测量方法相同的方式将PEDOT:PSS-EG MEA连接到阻抗测量仪器。
c.将PEDOT:PSS-EG MEA缠绕在圆柱形玻璃棒(直径:0.5 mm)上并测量电化学阻抗。
d.反复记录弯曲后透明PEDOT:PSS-EG MEA的电化学阻抗(1次,10次,100次和1000次)。
9.评估透明PEDOT:PSS-EG MEA与培养的皮质神经元的生物相容性。
a.准备怀孕的Sprague Dawley大鼠(胚胎18,DBL.Co)。
b. 处死大鼠,在制备的透明 PEDOT:PSS-EG MEA 上创建二维神经培养物。提取组织,并与神经组织分离试剂盒中的酶混合物一起研磨。
c. 用台盼蓝计数分离的活神经元。
d. 在制备的透明 PEDOT:PSS-EG MEA 上涂覆浓度为 100 μg/mL 的聚-D-赖氨酸。
e. 满足培养基条件,补充 2% v/v 的 B27 Plus、2 mM 的 Glutamax-I。同时用 CO2 培养箱将培养基温度保持在 37℃。
f. 评估体外(DIV)2 天和 6 天的细胞活力。用 1X PBS(1 μM CellTrace 钙黄绿素绿,AM)和 15 μM 碘化丙啶在 37℃ 下处理样品。
g.用 1X PBS 清洗样品。
h.用神经元特异性 3 类 β-微管蛋白抗体染色皮质神经元。
i.在 1X PBS 中的 4% w/v 多聚甲醛中将神经元固定在制造的样品上,在 25℃ 下放置一小时。
j.用 1X PBS 清洗样品三次。
k.用封闭溶液中的二抗(山羊抗小鼠偶联 Alexa Fluor 488,1:1000,A-11001)处理样品 2 小时。
l.用 1X PBS 清洗样品后,用 4′,6-二脒基-2-苯基吲哚(Invitrogen,1:1000)处理样品 1 小时。
图 3. 透明 PEDOT:PSS MEA 的光学、电化学、机械和生物相容性特性
(A) 透明神经电极阵列各种候选材料的光学透射率图。灰色线表示聚对苯二甲酸乙二醇酯 (PET) 基板的透射率,以供参考。
(B) 16 通道透明 PEDOT:PSS MEA 的电化学阻抗图(扫描频率:从 100 kHz 到 100 Hz)。
(C) 透明 PEDOT:PSS MEA 的机械弯曲测试导致的电化学阻抗变化。
(D) 第 2 天和第 6 天,不同基质(玻璃、PET、PEDOT:PSS-EG)上的大脑皮层神经元的活力。
(E) 第 6 天,对照基质(玻璃)和 PEDOT:PSS-EG 上的神经突(Tuj-1,绿色)和细胞核(DAPI,蓝色)的共聚焦荧光图像。比例尺,50 μm。
使用共聚焦激光扫描显微镜(Carl Zeiss,LSM700)获取样品的荧光成像。
3.4 使用电极记录体内癫痫样活动
时间:6 小时
将透明的 PEDOT:PSS MEA 以网格形式植入小鼠大脑皮层右侧,用于转基因小鼠(C57BL6 Thy-ChR2-YFP;8-10 周,25-30 克)的电生理记录。该电极阵列直接连接到可以记录信号的仪器上,从大脑接收到的信号链接到与该仪器兼容的软件。然后将匹鲁卡品注射到转基因小鼠体内,以询问使用我们的电极阵列记录癫痫发作活动的可行性。匹鲁卡品的详细剂量说明在另一项相关研究中介绍。在所有体内实验过程之后,信号通过陷波滤波器以60 Hz的频率进行滤波,高频范围(300 Hz-6 kHz)的信号也被滤波以获得清晰的局部场电位信号。在确定光遗传学和电生理学是否可以整合之前,进行了本实验,首先通过使用透明的PEDOT:PSS MEA测量癫痫样活动来检查神经信号记录的可行性。我们的电极阵列成功稳定地记录了与传统电极阵列相当的神经信号,表明它可以用作分析光刺激神经激活的工具。
10.进行动物手术,将透明的PEDOT:PSS-EG MEA植入动物模型的脑部。
a.准备雄性成年转基因小鼠。
b.腹腔注射麻醉聚氨酯(1.5 g/kg)。
c.准备立体定位仪。(图4A)。
图 4. 带有透明 PEDOT:PSS MEA 的转基因小鼠脑部电生理记录和光遗传学体内实验仪器设置。
(A) 立体定位仪 (B) 转基因小鼠脑部手术 (C) 实验小鼠的立体定位固定和设备植入 (D) 立体定位和激光仪器设置,用于同时进行电生理学和光遗传学 (E) 激光仪器 (F) 用于激光刺激的光学传感器 (G) 带有透明 PEDOT:PSS MEA 的转基因小鼠的光刺激(灯关闭)(H) 带有透明 PEDOT:PSS MEA 的转基因小鼠的光刺激(灯打开)。
d. 将麻醉小鼠固定在立体定位仪上,用仪器固定耳朵和鼻子。
e.为了露出小鼠的头骨,去除头上的毛发并在头皮上做一个切口(图4B)。
f.使用细电钻,水平露出2毫米,垂直露出2.5毫米的颅骨内脑组织(体感区右侧大脑皮层)(图4B)。
g.在颅骨上钻孔以植入导线后,植入导线参考电极(直径100μm)(体感区左侧大脑皮层)(图4B)。
关键:参考电极在与记录电极相邻的脑区的任何位置都是有效的。为了设置准确的参考电位,通常将金属螺钉固定在颅骨上并连接金属线,但如果参考电极直接接触脑组织则无关紧要。
11.准备脑记录仪并将其与透明PEDOT:PSS MEA连接。
a.准备脑部 Intan 记录仪(Intan RHD 2132 系统)(图 1H)。
b.将 ACF 与透明 PEDOT:PSS-EG MEA 连接。
关键:如果连接 ACF 和电极互连的部分连接不良,无论电极的电化学阻抗有多低,都无法获得高质量的神经信号。如果即使电极未损坏,电信号中也出现大量噪声,则很有可能是导电膜和阵列互连之间的连接不良。
c.将连接好的电极阵列的ACF端通过烙铁(160℃)热处理,连接到与Intan记录仪兼容的PCB上(图4C)。
d.将PCB连接到Intan记录仪和记录端口。
e.将参考电极连接到PCB上的仪器-动物模型参考连接器上(图4C)。
注意:当参考电极连接到从连接电极的PCB到记录仪的端口时,引脚会自动设置。
f.将Intan仪器接地,立体定位仪单独接地。
g.将电极轻轻放在小鼠右侧体感皮层的组织表面上。电极必须与脑组织直接接触。
h.用牙科水泥固定电极活动接触区以外的所有部位。
12.记录实验小鼠癫痫样电生理脑活动。
a. 运行 Intan 记录仪软件后,对要采集的信号应用陷波滤波器 (60 Hz) 和 0.1–6 kHz 的带通滤波器。
关键:对于记录为所有神经活动总和的局部场电位,它们对于 0.1 至 10 Hz 的激活区域有意义,并且单个神经元尖峰活动记录在 300 Hz 以上的高频范围内。应用带通滤波器时,根据研究人员打算分析的频带的神经活动对其进行修改。
b. 记录麻醉小鼠的静息电生理电位约 10 分钟。
c. 通过腹膜内注射给予 150 mg/kg 匹鲁卡品(加载时间:5 分钟)(图 5A)。
图 5. 使用透明 PEDOT:PSS MEA 对匹鲁卡品注射的癫痫样活动进行电生理记录。
(A) 转基因小鼠腹膜内注射毛果芸香碱示意图。
(B) 注射毛果芸香碱引起的诱发反应的电生理信号。
(C) 注射毛果芸香碱前后诱发的局部场电位 (LFP) 和频谱。
d. 腹膜内注射 100 mg/kg 毛果芸香碱,负荷时间为 10 分钟(图 5B)。
重要提示:如果给小鼠注射了高于适当剂量的毛果芸香碱,小鼠可能会在获取神经信号时因伴随癫痫样活动的各种症状而被处死。因此,必须根据实验小鼠的体重观察给药剂量。
e. 通过分析以 20 kS/s 采样率记录的原始数据,比较注射毛果芸香碱前后的诱发电位(图 5C)。
3.5 同时进行光遗传学和电生理学
时间:6 小时
在确认透明 PEDOT:PSS MEA 的记录可行性后,我们分析了光遗传学和电生理学是否可以整合。首先,该协议引入了微图案化过程,以使用 Au 创建与我们的电极阵列相同的电极形状。接下来,我们表明,当我们的电极阵列将光直接感应到电极表面时,转基因小鼠的光诱发电位明显高于传统金属电极阵列。这意味着当将相同强度的光刺激施加到小鼠的体感皮层时,透明 PEDOT:PSS MEA 通过电生理信号映射表现出更高的光传输效率(图 6A)。这些结果表明,透明 PEDOT:PSS MEA 即使在不同的光强度下也表现出优异的记录效率(237.09(2 mW)、115.55(1 mW)和 23.11 mW mm^(−2)(0.2 mW,方波频率:0.5 Hz,占空比:12.5%)(图 6B)。此外,为了检查电极中的光诱导伪影,我们将光施加到不含光响应蛋白通道视紫红质-2 (ChR2) 的野生型小鼠身上,并检查在神经记录过程中是否检测到特定伪影。虽然传统的金电极阵列在每次光刺激开始时都显示出清晰的光电伪影而不是局部场电位,但对于透明 PEDOT:PSS MEA 测量到的基于光的噪声可以忽略不计(图 6C)。
13. 制作传统的金 (Au) 电极阵列,以比较其与透明 PEDOT:PSS-EG MEA 的性能。
a. 清洁按照丙酮、异丙醇 (IPA) 和去离子水 (DI) 的顺序将 PET 薄膜基材压层。
b.在 PET 表面旋涂正性光刻胶 AZ 5214-E(旋涂速度:2000 rpm,40 s)。
c.将涂有光刻胶的 PET 基材放在 100℃ 的加热板上,固化约 2 分钟。
d.将带有电极图案的掩模放在光对准器上,并将其暴露在紫外线下约 8 s。
e.将仅部分暴露电极图案的样品在加热板上固化 2 分 30 秒。
f.将样品放在光对准器上后,将所有区域暴露在紫外线下约 15 s(无掩模图案)。
g.将适量的AZ 300MIF显影剂倒入培养皿后,将样品放入显影剂中,轻轻摇晃培养皿并显影(2分40秒)。
h.取出浸入显影剂中的样品,并用去离子水彻底冲洗。
i.去除水分后,将样品放入RIE室中,使用氧等离子体将表面处理为亲水表面约30秒。
j.将样品放入热蒸发器中并沉积50纳米厚的金。热蒸发器如图1I所示。
关键:沉积金时,由于与PET基板的粘附性差,该层可能会分层。在沉积金层之前,建议先沉积Cr层,厚度约为5纳米。
k.在玻璃盘中制备丙酮后,将沉积的金样品放在图案化的PET样品上。
l. 静置 10 分钟,直到 Au 下面的光刻胶被丙酮溶解,电极图案除外。
m. 将浸泡 10 分钟的样品放入超声波仪中,超声处理约 30 秒。
14. 用 UV 固化环氧树脂封装常规 Au 电极阵列。
a. 用 IPA 洗去超声处理吹走的 Au 残留物。
b. 用 UV 固化环氧树脂 (SU 8–2000.5) 旋涂样品 (3000 rpm,40 秒)。
c. 将样品放在 100℃ 的热板上 2 分钟。
d. 将样品放在光对准器上后,用样品上的记录位置图案覆盖光掩模。
e. 将其暴露在紫外线下 4 秒。
f.将样品再次放在加热板上,加热温度为 100℃,加热 2 分钟,30 秒,进行交联。
g.将样品浸入 UV 固化环氧显影剂中 1 分钟。
h.取出样品,用 IPA 清洗 40 秒。
i.将样品再次放在加热板上,加热温度为 120℃,加热 1 小时,进行硬固化。
15.进行动物手术,将透明的 PEDOT:PSS-EG MEA 植入动物模型的脑部。
a.准备雄性成年转基因小鼠(C57BL6 Thy-ChR2-YFP;8-10 周,25-30 克)。
b.腹腔注射麻醉聚氨酯(1.5 克/千克)。
c.准备立体定位仪和激光仪。实验装置如图 4D 所示。
d.将麻醉小鼠固定在立体定位仪上,用仪器固定耳朵和鼻子。
e.为了露出小鼠的头骨,去除头上的毛发并在头皮上做一个切口。
f.使用细电钻,水平露出2毫米,垂直露出2.5毫米,露出颅骨内的脑组织(体感区域的右大脑皮层)。
g.在颅骨上钻孔植入导线后,植入导线参考电极(直径100μm)(体感区左大脑皮层)。
关键:在动物实验之前,必须先使用光学传感器调整刺激神经的蓝色激光(473nm)的强度。光学传感器记录的激光光密度基于直径为105μm的光纤,是校准穿过PET基板后光强度的结果。
16.准备用于光遗传学的激光设备的光学传感器。
a.对于激光刺激,准备连接到直径为105μm的光纤的电源仪器和用于测量光强度的光学传感器。激光仪器和光学传感器的照片如图4E和4F所示。
b.使用光学传感器,调节电源,使光脉冲密度为115.55 mW/mm,占空比为12.5%。
c.准备脑Intan记录仪(Intan RHD 2132系统,洛杉矶)。
d.连接ACF和透明PEDOT:PSS-EG MEA。
e.通过使用烙铁(160℃)进行热处理,将连接的电极阵列的ACF端连接到与Intan记录仪兼容的PCB。
f.将PCB连接到Intan记录仪和记录端口。
g.将参考电极连接到PCB上的仪器-动物模型参考连接器。
h.将Intan仪器接地,并将立体定位单独接地,以减少动物模型中的运动伪影。
i.将电极轻轻放在小鼠右侧体感皮层的组织表面上。电极必须与脑组织直接接触。
j.使用显微镜,准备用于激光刺激的光纤,将其直接放置在电极上方。图 4G 和 4H 显示了光刺激和直接在电极上打开/关闭激光的放大图像。
k.当以刺激频率(0.5 Hz,占空比:12.5%)给予光刺激时,使用 Intan 记录仪器测量光引起的诱发电位。
l.以与上述相同的方式使用常规 Au MEAs 光刺激进行电生理记录。
图 6. 使用常规金属电极阵列和透明 PEDOT:PSS MEAs 对转基因小鼠进行同时电生理学和光遗传学研究。
(A)16 通道常规金属电极阵列(左)和透明 PEDOT:PSS MEAs(右)对转基因小鼠大脑进行光刺激后的电生理映射结果。
(B) 转基因小鼠光刺激后光诱发电位强度比较,其中常规金属电极阵列(左)和透明 PEDOT:PSS MEA(右)。
(C) 激光照射野生型小鼠大脑后,常规金属电极阵列记录的光电伪影信号。黑色虚线表示刺激开始。
四、预期结果
使用 PEDOT:PSS 的无金属层透明电极阵列在用作可植入设备时可作为与光遗传学整合的关键工具。与使用传统电镀方法沉积的 PEDOT 不同,本方案中介绍的制造工艺可以克服光刺激期间可能出现的光电伪影和有限的光透射等缺点。在本方案中,通过 EG 后处理确保了适合电生理记录的电化学阻抗,从而改善了 PEDOT:PSS 相对较低的电导率。此外,还提出了利用超声剥离法实现 50 μm 以内的精细图案的高密度电极阵列的可能性。
在该方案中,首先分析了 PEDOT:PSS 电极阵列的低电化学阻抗、高透光率和机械稳定性。在确认电极阵列具有足够的性能插入活体后,对转基因小鼠进行了癫痫样活动测量,以确认电极阵列的电生理记录可行性。结果,我们成功地测量了毛果芸香碱注射引起的 LFP,没有任何噪音。接下来,对于同时进行神经记录和光遗传刺激,我们比较了透明 PEDOT:PSS MEA 和传统金电极阵列的光传输效率,并比较了转基因小鼠的神经激活情况。结果证实,即使在相同的蓝色激光 (473 nm) 刺激强度下,传统的金电极阵列也会吸收大部分光,因此几乎不会激活脑神经活动。相比之下,透明的 PEDOT:PSS MEA 显示出清晰的光诱发电位,因为它们保持了足够的透明度来传输大部分光。
最后,对不受光神经激活影响的野生型小鼠进行光刺激,同时用两个电极阵列进行记录,分析光电伪影。在野生型小鼠的情况下,蓝色激光刺激不应观察到特殊的诱发电位,每次刺激开始时看到的峰值表示由金属层引起的光电伪影。值得注意的是,在传统的金电极阵列中观察到被光电伪影污染的神经信号,而在透明的PEDOT:PSS MEA中仅记录了可忽略不计的噪声。这些结果表明我们的工作可以在电生理学和光遗传学的整合中发挥关键作用,使其成为未来临床应用和神经回路分析的潜在工具。
五、局限性
在制造电极阵列后,如果在工艺环境湿度较高的情况下不进行确定记录位置的封装,则由于PEDOT:PSS层吸收水分,电极性能可能会下降。虽然电极的电化学阻抗不会降低性能到对电生理记录产生关键影响的程度,但它可能不利于获得高质量信号,因此在设备制造工艺环境中需要谨慎。此外,电极阵列与记录仪器的各向异性导电膜之间的连接不稳定,可能导致记录信号采集不良,与设备性能无关。
六、故障排除
问题 1
难以用超声波剥离工艺对微电极进行图案化(与步骤 1e-1i 相关)。
如果电极没有通过光刻实现 20 μm 内的精细图案,最可能的原因是三个问题:光刻胶的化学材料变化、由此产生的紫外线曝光时间变化以及显影剂的显影时间。如果没有正确观察根据溶液性质变化的曝光时间,则有可能所有预定图案都可能消失或与电极的互连线可能断开。
潜在解决方案
如果用光学显微镜观察制作的电极图案,发现图案模糊且结构宽度远大于预定设计,则需要进一步增加曝光时间。相反,如果图案比现有设计更暗,但图案之间的间距非常窄,则应减少曝光时间。在使用显影剂的情况下,它不取决于指定的显影时间,当目视确认光刻胶的红色溶解材料已完全从电极表面消失时,用去离子水彻底清洗。
问题 2
SU 8–2000.5 的特性对周围环境(温度、湿度等)变化敏感(与步骤 4b-4h 相关)。
在 SU-8-2000.5 封装以确定电极传感位置期间,可能会发现各种意想不到的现象。例如,有些情况下 SU-8-2000.5 未均匀地旋涂在已完成的设备上,或者未按照称为配方的显影时间正确图案化。
潜在解决方案
对于 SU-8 系列负性光刻胶,其特性会根据周围环境的温度和湿度而敏感地变化。换句话说,有些情况下,只有使用与现有配方不同的方法才能实现正确的图案化。在进行图案化以确定电极的传感位置时,如果记录位置比预期的要小,建议将紫外线曝光时间减少 1-2 秒。或者,还建议将显影时间减少约 20 秒。如果 SU-8 未均匀地旋涂在电极上,建议首先通过温和的 O2 等离子处理将电极表面更改为亲水表面。
问题 3
来自实验装置的外部设备的电噪声(与步骤 11f 相关)。
尽管 Intan 记录仪接地充分,参考电极插入正确,神经记录过程中仍可能经常出现不必要的电噪声。这很可能是由于外部电子设备可能穿透噪声,或与 Intan 记录仪兼容的 PCB 存在缺陷。
潜在解决方案
如果接地充分后仍继续出现电噪声,则很可能是 PCB 本身连接不良。在电极性能得到完美保证的前提下,应重新检查所有 Intan 记录仪是否存在连接不良,并将外部电子设备放置在较远的位置。
问题 4
当立体定位坐标没有准确指定时(与步骤 11g 相关)。
当将电极植入转基因小鼠的大脑时,请务必在进行实验之前检查要插入的大脑区域的立体定位坐标。如果电极放置在大脑表面已经过了一段时间,大脑表面组织中的水分可能会变干并粘附在电极上。在这种情况下,请注意,如果立即将电极从大脑表面移除,可能会发生组织损伤或疤痕。
潜在的解决方案
如果研究人员想在脑电图网格升至大脑表面后改变立体定位坐标,首先在电极周围撒上足够的 PBS 液滴,为周围区域提供水分。之后,考虑到电极和组织之间的狭窄,应将电极从再次放置在所需区域的表面缓慢移除。
问题 5
区分外部噪声和匹鲁卡品诱发电位(与步骤 12c 相关)。
当注射匹鲁卡品检查电生理记录可行性时,可能会得到无法清楚区分测量信号是匹鲁卡品引起的诱发电位还是简单噪声的数据。
潜在解决方案
区分外部噪声和来自大脑的神经信号的最清晰方法是分析频率范围内的模拟信号。当匹鲁卡品引起的大脑活动开始出现时,可以使用频率幅度分析来区分噪声和失神发作。