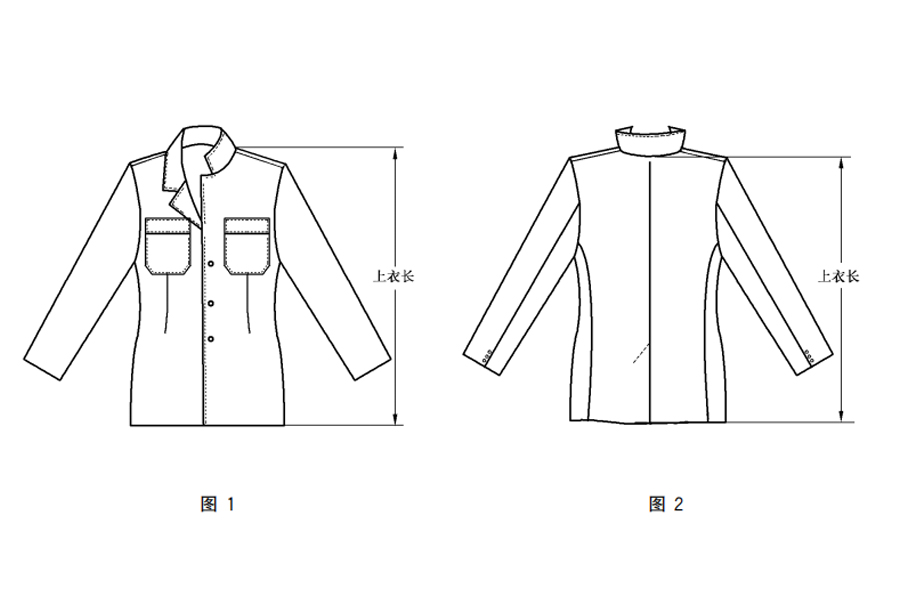
如果你关注康复医疗或者科技新闻,最近几年肯定没少听到“外骨骼机器人”这个词。听起来特别科幻,像是从钢铁侠电影里走出来的装备。但在我们医疗器械行业里,它已经是一个实实在在、正在快速走进医院和康复中心的产品。简单来说,外骨骼康复机器人就是一种穿在人体外部的机械装置,通过精密的传感器、驱动器和控制算法,来辅助或增强使用者的肢体运动能力。在康复领域,它的核心使命就是帮助那些因中风、脊髓损伤、脑外伤或骨科手术后导致运动功能障碍的患者,重新“学习”走路、训练手臂,恢复生活自理能力。
那么,这么个“高科技玩意儿”,在咱们国家到底算不算医疗器械?答案是肯定的,而且它被管得明明白白。根据国家药品监督管理局(NMPA)发布的《医疗器械分类目录》,外骨骼康复机器人主要被归在 19“医用康复器械” 这个大门类下。具体来说,它属于 19-02“运动康复训练器械” 中的 “关节训练设备” 或 “步态训练设备”。目前,这类产品绝大多数被划分为第二类医疗器械进行管理。
这里我得插一句,很多刚入行的朋友容易混淆“一类、二类、三类”的区别。你可以这么理解:风险等级越高,管理越严格。一类是风险程度低,实行常规管理(比如手术刀、纱布);二类是具有中度风险,需要严格控制管理以保证其安全有效(比如血压计、我们说的外骨骼);三类是风险程度高,必须采取特别措施严格控制(比如心脏起搏器、人工关节)。所以,外骨骼作为二类器械,意味着它的研发、生产、临床试验和上市审批,都有一套非常严格和完整的法规流程要遵循,绝不是做个样机就能卖的。
为什么分类这么重要?因为它直接决定了你产品后续的“人生路径”。你是走创新医疗器械的绿色通道,还是按常规路径注册?你的产品检测要依据哪些标准?你的临床评价是该做临床试验还是可以用同品种比对?这些问题的起点,都在于准确的分类。我见过有团队一开始没搞清楚,产品设计都快定型了,才发现分类定错了,导致前期很多工作推倒重来,那真是欲哭无泪。所以,我的第一个建议是:动手研发前,第一件事就是去国家药监局医疗器械标准管理中心的网站,或者直接去国家药监局数据查询页面,把分类目录翻个底朝天,确认好自己的产品子目录和预期用途,必要时甚至可以申请分类界定,拿到官方的书面意见,这是最稳妥的。
产品分类搞清楚了,接下来就要面对一堆让人头疼的标准和规范。对于外骨骼机器人来说,目前最核心、也是你必须攻克的一座大山,就是 YY 9706.278-2023《医用电气设备 第2-78部分:康复、评定、代偿或缓解用医用机器人的基本安全和基本性能专用要求》。这个标准名字很长,但地位极高,你可以把它理解为医用机器人领域的“根本大法”。
这个标准是YY 9706(医用电气设备) 系列标准中的一个专门部分,而YY 9706系列又等同采