Julia Mario, MDa,*, Shambhavi Venkataraman, MDb, Valerie Fein-Zachary, MDb, Mark Knox, MBBChb, Alexander Brook, PhDb, Priscilla Slanetz, MD, MPHb
哈佛医学院,波士顿,马萨诸塞州,美国 美国马萨诸塞州波士顿贝斯以色列女执事医疗中心放射科
摘要
目的:我们的目的有两个。首先,我们试图确定切除乳腺癌标本的2个正交定向视图与单个无定向视图相比是否可以提高手术切缘评估。其次,我们试图确定与单纯2D乳房x线摄影相比,3D断层合成术是否可以改善手术切缘评估。
材料和方法:使用4种方案对41例连续标本进行前瞻性成像:在样本单元上获取的单视图无方向二维图像(1VSU),在样本单元上获取的2张正交方向二维图像(2VSU),在乳房x线照片单元上获取的2张正交方向二维图像(2V2DMU),在乳房x线照片单元上获取的2张正交方向三维图像(2V3DMU)。三名乳腺成像师随机评估41例标本的手术切缘。手术切缘按组织病理学判定为金标准。
结果:1VSU平均曲线下面积(AUC)为0.60,2VSU为0.66,2V2DMU为0.68,2V3DMU为0.60。2VSU与1VSU的auc比较显示2VSU提高了诊断的准确性;然而,这一差异仅在读者3组有统计学意义(0.73 vs 0.63, P .0455)。比较2V3DMU和2V2DMU的auc显示了混合的结果,读取器1显示了更高的准确性(0.72 vs 0.68, P .5984),而读取器2和3显示了降低的准确性(0.50 vs 0.62, P .1089)0.58 vs . 0.75, P .0269)。
结论:与1VSU相比,2VSU显示手术切缘预测的准确性有所提高,尽管这对所有读者来说并没有统计学意义。3D断层合成不能改善手术切缘评估。
保乳治疗(BCT),或乳房肿瘤切除术后进行全乳放射治疗,已被证明与乳腺切除术治疗I期和II期浸润性乳腺癌的效果相当[1e3]。然而,为了BCT成功,必须以阴性手术切缘切除肿瘤,以确保肿瘤完全切除。当标本[4]边缘的癌细胞上有墨汁时,局部肿瘤复发的风险至少是原来的两倍。组织学上可见组织学阳性边缘[5],再切除率10%e57%视情况而定机构的实践和期望的负边际宽度[6,7]。对于什么构成安全边缘缺乏共识也导致许多患者接受二次手术。重复的手术会增加医疗费用,给病人带来更多的压力,并可能导致不理想的美容结果。
在筛查性乳房x线摄影广泛使用的时代,大多数切除的癌症是无法察觉的,因此需要图像引导程序,通过活检获得术前诊断,并指导手术。大多数成像中心通常在活检部位放置一个金属夹子来标记指标性病变。术前图像引导的金属丝定位目标病变(如果活检后仍存在)或定位夹,现在通常用于精确切除病变和减少切除正常组织的数量。事实上,美国So- city of Breast Surgeons关于乳腺癌肿瘤切除边缘的立场声明(2013)声称,必须通过x光检查确认所有无法触及的、图像检测到的病变都被切除了,而且手术中必须将标本成像结果直接告知外科医生。美国乳腺外科学会也建议病理学家可以获得标本图像。
外科标本成像评估目标病变是否完全切除通常采用二维乳房x线摄影,如果手术前超声能清楚地识别病变,也可以使用超声。传统上,标本的乳房x线照相术是使用专用标本单元或数字乳房x线照相术单元完成的,获取单个视图或两个正交视图。大多数的做法获得一个单一的无方向的观点切除的组织。然后,放射科医生与外科医生沟通目标病变是否已切除,并通常评价病变到边缘的距离。关于两种观点是否优于一种观点的研究显示了混合的结果[10,11]。而且,据我们所知,关于边际评价中2种观点是否优于1种观点的研究相对较少。
最近,三维(3D)数字断层合成(DBT)已经显示出作为一种优于2D乳房x线摄影的诊断工具的前景,因为它消除了组织重叠。多项研究表明,在筛查和诊断人群中,使用DBT可以提高病变的检出率和改善边缘评估[12e15]。此外,DBT在评估乳腺致密组织[15]时被认为是一种优越的技术。致密的乳腺组织可能倾向于更高的再次切除率。一项研究显示,致密乳腺组织有3.6个[6]重复手术的优势比,而在另一项研究中,11名致密乳腺女性中有10名(91%)在[16]切缘阳性的基础上被建议进行重复手术。
材料和方法
这项前瞻性研究得到了以色列贝斯女执事医疗中心机构审查委员会的批准,并符合健康保险可携性和责任法案。我们机构内部资助了这项研究。没有外部或行业资助。.
患者包容
从2013年7月1日至2014年1月9日,使用4个研究方案对70例术前诊断为导管原位癌(DCIS)、浸润性乳腺癌或其他可疑影像学结果而接受乳房保留手术的患者连续手术标本进行了成像。术前诊断基于图像引导下经皮组织活检。当标本从手术室取出时,以连续的方式成像;然而,偶尔,由于DBT单元的限制,标本不能成像,因此,不包括在研究中。最终手术病理为良性的影像标本(n 22)不包括在研究中,因为切缘评估没有临床意义。另外9例因成像不完全而被排除。39例患者共41例乳腺癌标本纳入分析。
标本成像过程
每个患者术前都在乳腺放射科对乳腺病变进行了金属丝定位。手术切除后,切除的组织立即送往放射科,由技术人员进行常规2D成像。放射科医生评估标本的x光片,并将检查结果告知外科医生,外科医生随后进行伤口闭合或立即再次切除。此时此刻,保存在密封塑料生物危害袋中的标本,由3名调查人员中的1名(j.m., p.s.和M.K.)使用4种不同的方法对其进行了成像。然后将标本送往病理学家,病理学家稍后对标本进行检查和边际评估。术中病理学家未进行肉眼检查。随后,3名委员会认证的乳腺放射科医师独立审查了研究图像,以评估每个标本的边缘状态。
标本定位,成像协议和技术
使用外科缝合完成标本定位,短针标记上侧面,长针标记侧面。对于第一幅图像,短针朝上(远离探测器板),长针朝侧面(图1)。对于第二幅图像,标本旋转90〇,使短针朝成像仪,长针继续朝侧面。
所有手术标本均使用常规方案以及3个附加方案成像,共4个图像集(图2),如下图所示。
单视图标本单元(1VSU)(常规方案)
在一个专门的标本单元(piXarray 100 Digital samples Radiography System, 2009;Bioptics Inc,图森,阿斯利康)。技术人员将试样放置在检测板上,不考虑方向,然后使用预先设定的kV和mAs值拍摄单幅图像,根据试样的大小需要手动调整。kV为28e31, ma为8e10。使用标准供应商特有的放大倍率。标本未被压缩。这个成像协议是我们机构目前的做法。
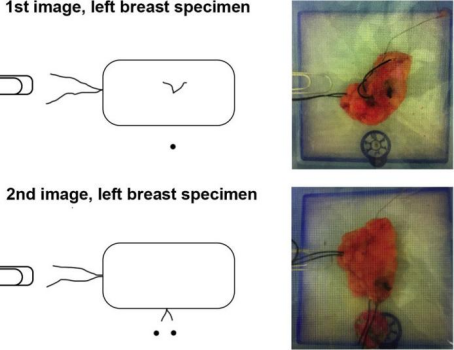
图1所示。标本方位图。左乳房标本在检测板上自上而下的拍照和绘图。短线迹为上位,长线迹为侧位。在第一张图片中,长针朝侧面(在这种情况下是左边,因为它是左乳房标本),短针朝上(远离检测板)。在第二幅图中,标本已朝成像仪向上旋转90〇度,使短针现在面向成像仪,长针继续面向侧面。第一张图像用1bb(蓝色贴纸)标记,表示后侧面(胸壁),用回形针标记侧面。第二幅图用2个BBs(蓝色和粉色贴纸)表示上侧面,用回形针表示侧面。这个数字的彩色版本可以在http://carjonline.org/上找到。
双视图标本单元(2VSU)
在专用的样品单元上获得两个正交的、定向的二维图像。研究人员将试样定位在探测器板上,并拍摄第一幅图像。然后将标本旋转90°,使用相同的成像参数获得第二张图像。使用预先设定的放大倍率,kV和mAs值。对于较大的样品,调整kV和mAs。标本未被压缩。
双视图3D乳腺x线片(2V3DMU)
在DBT单元(Selenia Dimensions System, 2012;Hologic Inc, Marlborough, MA)。为了达到与标准样品单元相同的放大倍数,使用了一个平台将样品从检测板上抬起。首先将两个屏蔽压片(分别为24cm – 29cm和18cm – 24cm)堆叠在检测板上。然后,研究人员将标本置于顶部桨叶表面,在拍摄图像之前,使用10厘米的接触桨叶从上方轻轻地压缩标本。然后重复该步骤得到正交图像。手动设置kV为28,并根据需要进行微调。mAs是手动设置的,根据样品的大小在75e100范围内。
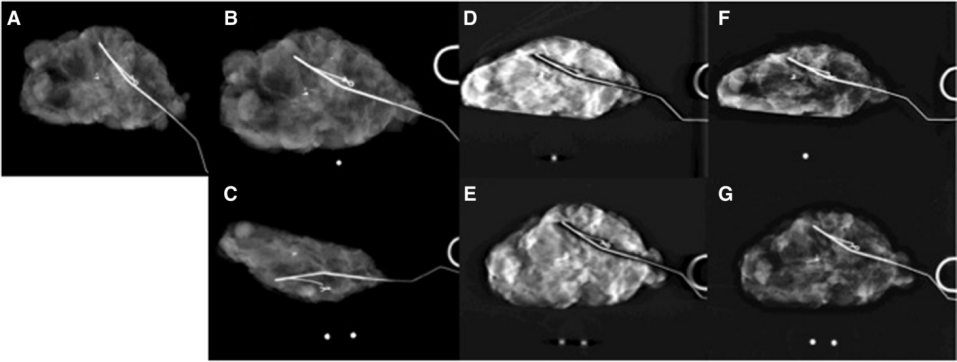
图2。标本成像采用4种不同的研究方案。81岁女性,术前对右侧乳腺钙化肿块进行针定位,初步活检显示为导管原位癌。在这种情况下,所有的读者都把所有的模态的边缘称为积极的;然而,注意在C面,钙化更明显地延伸到下缘。最终的手术病理显示浸润性癌,下缘呈阳性。患者最终没有再次切除。(A)在样本单元上获取的单视图无方向二维图像。(B, C)在样本单元上获得的两个正交的、定向的二维图像。(D, E)在乳房x线片上获得的两个正交的、定向的三维图像。(F, G)在乳房x线片上获得的两个正交的,定向的二维图像。
二视图二维乳腺x线片(2V2DMU)
在DBT单元上获得了两个正交的、定向的二维图像。使用与2V3D相同的成像协议;然而,数字设置被改为2D图像,而不是3D图像。
数据收集
分别有21年、27年和25年经验的三位乳腺成像师(S.V.、V.F.Z.和P.J.S.)使用4组研究方案图像集独立评估了每个标本的切缘状态,但对最终手术切缘状态不知情。每个读者都看不到其他读者。每个组织病理的最终切缘状态被认为是金标准。图像集按随机顺序读取,每个阅读器的每个协议读取会话之间有4周的冲洗期。标本的阅读顺序在每个图像集内也是随机的。
放射科读者记录切缘状况和最近切缘。在我们的研究中,我们将切缘定义为小于1 mm为阳性,小于1-5 mm为闭合,大于5 mm为阴性。虽然我们机构的病理部门将肿瘤细胞上有墨迹的边缘定义为阳性,但我们认为,为了研究目的,将边缘定义为1mm的阳性边缘可以让我们更好地比较x线摄影和显微镜标本检查。更符合我们外科同事的临床实践。所有对射线图像的测量都是使用供应商指定的测量工具进行的,该工具可在图像存档和通信系统或Hologic观察站上使用。每个放射科医生都被提供了一个标本定位示意图,以便在检查图像(前、后、内侧、外侧、上、下边缘)时对每个切缘进行正确的识别。作者J.M.将读者资料与最终的手术切缘状态相关联。病理学家报告癌细胞与每6个边缘的距离,单位为毫米。为了正确地比较放射科医生读取数据和病理数据,我们使用提供的病理测量距离将病理边缘状态转换为符合我们的研究定义。例如,如果病理学家提示距内侧缘0.7 mm处存在癌,因此报告为“阴性”,那么在我们的研究中,病理内侧缘为“阳性”。
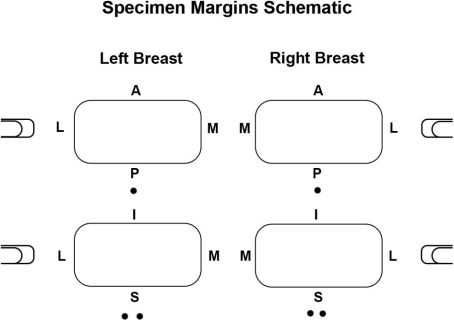
图3。标本利润率示意图。所有放射科医生在阅读标本图像时,都使用此示意图作为参考工具,以正确识别每个边缘。BBs和回形针被用来标记页边空白处。第一张图像用1bb标记后侧面(胸壁),用回形针标记侧面。第二张图用2个BBs表示上侧面,用回形针表示侧面。A前¼,P后¼,L外侧¼,M内侧¼,S上¼,I下¼。
结果
39例患者中41例为恶性肿瘤。两名患者各提供来自同一乳房不同部位的2个不同标本。所有患者均为女性,平均年龄为60.66岁,标准差为12.67。41例标本中,DCIS 11例,浸润性癌30例。组织病理学检查:25/41为阳性(44%)例立即再次切除,12/41例(29%)因发现标本边缘(0 mm)有肿瘤,需稍后再次切除。表1详细列出了患者的其他特征。
病理组织学阳性病例的标本特征见表2。研究的41例标本中,15例同时患有DCIS和浸润性癌症。在这15例患者中,11例DCIS离切缘最近(例如DCIS 1mm,浸润性2.5 mm), 2例浸润性癌离切缘最近,2例浸润性癌3名读者之间的读者间协议对4种模式是公平的,Fleiss kappa统计为显示了相对较低的准确性,解释范围从毫无价值到公平(表3)。平均AUC最高的是2V2DMU(0.68),其次是2VSU(0.66),然后是2V3DMU(0.60),然后是1VSU(0.60)。每个读者的每一种形态的敏感性和特异性如图4所示。敏感性、特异性、阳性预测值(PPV)和阴性预测值(NPV)见表4。使用所有实验模式的平均敏感性显著更高(2V2DMU, 64%;2V3DMU为60%,2VSU为57.33%),而传统1VSU为42.67%。常规1VSU模式的平均特异性最高(77.08%)。2VSU和2V2DMU模式的平均PPV和NPV均最高。
与常规二维成像相比,断层合成技术是否改善了影像学边缘评估?
通过阅读器比较2V3DMU和2V2DMU的auc显示了混合结果,阅读器1显示了更高的准确性,而阅读器2和3显示了更低的准确度(表5)。2V3DMU的平均灵敏度低于2V2DMU (60% vs 64%,(表4)。通过McNemar检验比较2V3DMU和2V2DMU的敏感度显示出混合结果,阅读器1显示出更高的敏感度,而阅读器2和3显示出更低的敏感度(表6)。2V3DMU的平均特异性明显低于2V2DMU (60.42% vs 72.92%,McNemar检验比较2V3DMU与2V2DMU的特异性总体下降或相等,特异性无统计学意义(表7)。
通过读取器比较2V3DMU和2VSU的auc,结果相似,读取器1的准确率提高,而读取器2和3的准确率降低(表5)。2V3DMU的平均灵敏度略高于2VSU (60% vs 57.33%,(表4)。通过McNemar检验比较2V3DMU和2VSU的敏感度,读者1显示出更高的敏感度,而读者2和3显示出更低的敏感度(表6)。2V3DMU的平均特异性明显低于2VSU (60.42% vs 75%,(表4)。比较2V3DMU与2VSU特异性的McNemar检验显示,所有检测者的特异性均降低;然而,这些差异没有统计学意义(表7)。
与1VSU和2V3DMU相比,在专用规格单元(2VSU)和乳房x线片单元(2V2DMU)上的双视角成像都有最高的PPVs和最高的npv(表4)。
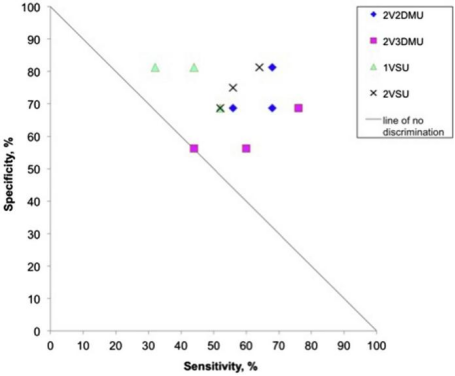
图4。对每一种形态和读者的敏感性和特异性的总结。这个数字的彩色版本可以在http://carjonline.org/上找到。
讨论
BCT是目前公认的早期乳腺癌治疗方法。为了使BCT有效,切除的肿瘤边缘应为负的。虽然切缘状态和复发风险之间的关系并不确切,但在初次手术时或以后再次切除时,都有可能获得阴性切缘。当第一次手术预示着有积极的边际时,通常建议进行第二次手术。再切除与更糟糕的美容结果有关,还会增加医疗保健费用,延迟放射治疗,并给患者带来显著的额外压力。
关于构成适当负边际的定义历来存在争议,范围从墨水处无癌到1cm内无癌[17e19]。然而,Moran等人在2014年发表了关于肿瘤边缘的明确指南,此前进行了一项全面的荟萃分析,结果显示肿瘤细胞上无墨色与低局部复发率相关。这些由外科肿瘤学会和美国放射肿瘤学会提出的共识指南,将浸润性肿瘤或DCIS的墨迹定义为阳性边缘,而将阴性边缘定义为无墨迹。此外,Morrow等人(2016)最近发表了外科肿瘤学会、美国放射肿瘤学会和美国临床肿瘤学会的明确共识指南,建议DCIS和微浸润[21]的DCIS切缘宽度为负2mm。欧洲医学肿瘤学协会同样将浸润性肿瘤或DCIS的切缘定义为阳性,而将阴性切缘定义为无墨,并进一步说明原位疾病的切缘最好为2mm(2015)。









