2014年第9期
(总第110期)
内容提要
一、美国FDA发布关于Medtronic Neurosurgery公司制造的Medtronic Duet体外引流及监测系统的召回通知
二、美国FDA发布关于Vascular Solutions公司制造的Langston V2双腔导管的召回通知
三、美国FDA发布关于Ventlab公司制造的Ventlab人工复苏器的召回通知
四、英国MHRA发布关于Roche公司制造的Accu-Chek血糖仪的警示信息
五、英国MHRA发布关于乳房植入物的警示信息
六、英国MHRA发布关于DePuy Synthes公司制造的Synthes创伤外固定系统的警示信息
国家药品不良反应监测中心
国家食品药品监督管理局药品评价中心
http://www.cdr.gov.cn
一、美国FDA发布关于Medtronic Neurosurgery公司制造的Medtronic Duet体外引流及监测系统的召回通知
召回级别:I类
召回发起日期:2014年6月9日
召回产品:
Medtronic Duet体外引流及监测系统(EDMS)用于对脑脊液(CSF)进行体外引流及监测,以及对颅内压(ICP)进行监测。该器械仅在经过培训人员监督下用于患者全天候监测与引流。部分产品编号为46913、46914的注射连接部件,产品编号为46915、46916的注射连接部件和脑室导管,产品编号为46917的注射连接部件和腰椎导管被要求召回,这些受召回影响的产品于2013年3月15日至2014年2月28日制造,2013年4月10日至2014年5月19日进行分销。
召回原因:
生产企业召回这些医疗器械是因为与患者连接的管路可能与管路接头分离。生产企业称,当对患者管路频繁操作时,如在连接处频繁进行注射或采样操作,管路更容易断开。器械失效后可能引起空气在颅内集聚(颅腔积气)、感染(如脑膜炎、脑室炎和脑炎)、CSF引流过度或不足,这些情况可能导致严重的不良健康后果甚至死亡。
采取措施:
生产企业于2014年6月9日向客户发送了“医疗器械紧急召回函”,函件中对受影响产品、相关问题以及需采取的措施进行了说明。企业要求客户停止使用受影响产品并将所有未使用的器械返回至Medtronic Neurosurgery公司,填写并返回随函件所附的“客户产品责任表”,如果正在使用受影响产品,则应根据使用说明书确认所有连接均牢固且无泄漏现象。
二、美国FDA发布关于Vascular Solutions公司制造的Langston V2双腔导管的召回通知
召回级别:I类
召回发起日期:2014年5月27日
召回产品:
Langston V2 双腔压力监测导管用于医学成像试验(血管造影研究)期间向患者血管内输送造影剂,从而使临床医生得以看清体内结构。该器械还可用于测量血管内压。于2014年1月至2014年4月制造, 2014年3月至2014年5月进行分销的部分5540型与5550型Langston V2 双腔压力监测导管被要求召回。
召回原因:
生产企业收到一些报告提示Langston V2双腔导管在使用过程中内导管与器械接头会分离,这可能要求施行手术,将断离的部件从患者血管系统中取出。
使用被召回的器械可能会造成严重不良健康后果甚至死亡。
采取措施:
Vascular Solutions公司于2014年5月23日向其客户发送“医疗器械紧急召回函”。该函件指出了相关问题以及受召回影响的特定产品,同时建议客户找出所有受影响器械并将其置于安全区,填写并返回随函件所附的“VSI客户存货表”。Vascular Solutions将对返回的器械进行更换。
三、美国FDA发布关于Ventlab公司制造的Ventlab人工复苏器的召回通知
召回级别:I类
召回发起日期:2014年5月16日
召回产品:
Ventlab人工复苏器为一次性器械,用于为无法自主呼吸的患者提供暂时性支持。器械仅供经过心肺复苏术(CPR)培训的人员以及紧急救援人员使用,主要用于医院、诊所。要求召回的器械于2013年1月10日至2013年7月1日制造并分销,涉及商品名为Airflow Bag、Breath Tech Bag、Provider Bag、STAT-Check Bag、Safe Spot Bag、V-Care Bag、Medline Bag、RescuMed Bag、VT1000 Kit等多个复苏器系列。
召回原因:
复苏器内鸭嘴阀可能粘住,从而阻止空气经阀进入患者呼吸道。若患者未吸入氧气或治疗延迟,则可能产生危及生命的健康后果,包括组织供氧不足(低氧)、呼吸太浅或太慢(肺换气不足)甚至死亡。目前该公司收到一例因复苏器失效导致患者需要医学介入的伤害报告。
采取措施:
Ventlab公司于2014年5月13日发布了一篇新闻稿,宣布召回受影响的Ventlab复苏器。拥有受影响复苏器的用户应停止使用并立刻联系Ventlab公司返回这些产品。
(美国FDA网站)
四、英国MHRA发布关于Roche公司制造的Accu-Chek血糖仪的警示信息
发布日期:2014年7月9日
警示产品:
Roche制造的Accu-Chek血糖仪与试纸(Compact型)、Accu-Chek血糖仪与试纸(Active型)、Accu-Chek血糖仪与试纸(Mobil型)。外观如图所示:
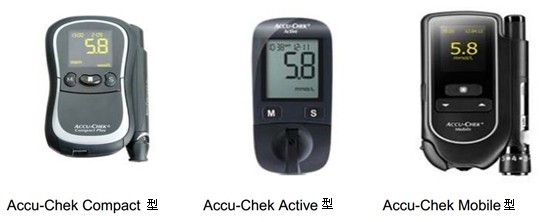
警示原因:
上述三种产品用于检测患者血糖时,如果患者正接受的头孢曲松治疗,会给出提示低血糖的错误血糖值。
采取措施:
Roche已更新了上述器械的产品使用说明书并发布了现场安全通告(FSN),并将其分发给专业医护人员。通告中明确指出,临床应用上述产品的医护人员以及药剂师、微生物学专家、门诊抗生素用户应分辨接受头孢曲松治疗的糖尿病患者,并告知这些患者在头孢曲松治疗持续期内切勿使用上述三种血糖仪,在其治疗期间应使用其他替代器械。
五、英国MHRA发布关于乳房植入物的警示信息
发布日期:2014年7月10日
警示产品:
所有类型与型号的乳房植入物。
警示原因:
FDA在对1997年1月至2010年5月所发表的科学文献进行评审后鉴别出全球共有34例女性(植有乳房植入物)患有间变性大细胞淋巴瘤(ALCL),另外FDA不良事件报告体系还包含17例女性(植有乳房植入物)患有ALCL的报告,因此FDA于2011年1月份发布了 “FDA医疗器械安全通告:植入乳房植入物女性的间变性大细胞淋巴瘤(ALCL)报告”。欧盟委员会及欧盟新兴及新鉴定健康风险科学委员会(SCENIHR)于2014年5月份发表了一份有关PIP硅胶乳房植入物的最终报告,SCENIHR鉴定出世界范围内共有130例植有各类乳房植入物的患者患有ALCL。对于世界范围内500-1000万植有乳房植入物的女性而言,报道的情况只占很小一部分。
自2011年2月发表MDA/2011/017要求医护人员报告植有乳房植入物女性的间变性大细胞淋巴瘤(ALCL)病例后,在英国已经收到3例ALCL报告。
采取措施:
MHRA将通过各种渠道继续收集这类问题的相关信息并深入分析,以此来构建该种与乳房植入物有关的罕见疾病的更加完整的发生率概图。MHRA发布该警戒通告的目的在于进一步鼓励医护人员报告植有乳房植入物或乳房植入物已取出女性ALCL病例。
MHRA同时也建议相关单位及个人,如乳房再造与丰胸手术单位及医疗主管、医护人员、放射与内科肿瘤学部等无需改变当前好的局面,在移植、一般的放射性检查、核磁共振检查时按例行方式进行,如果有女性咨询相关疾病则应告知对方ALCL是一种罕见癌症,只要在早期检测出则可以治愈。强烈建议有乳房植入物的女性对乳房和叶腋(腋下)坚持做自我检查,看是否发生变化,如肿块、肿胀或畸变,若有问题应该咨询医生。
六、英国MHRA发布关于DePuy Synthes公司制造的Synthes创伤外固定系统的警示信息
发布日期:2014年7月23日
警示产品:
部件号分别为292.400和395.578的所有批次Synthes创伤外固定系统(小型、中型、牵张成骨(DO)环、大型)。
警示原因:
根据将产品适用MR条件确定为MR Safe(MR安全)、MR Conditional(条件性磁共振兼容)、MR Unsafe(MR不安全)的要求,金属器械不再定位为MR Safe(MR安全)器械,Synthes外固定系统(小型、中型、大型与DO环)也不再适用MR Safe(MR安全)标识。于磁共振成像(MRI)孔内或孔外缘7cm内使用Synthes外固定系统(无论该系统标为“MR Safe”还是“MR Conditional”)可能会导致器械升温超过6℃,这可能会造成软组织热损伤或骨损伤,从而给患者带来不适或疼痛。因此对这些器械使用说明书进行了修改,这些器械现在被确定为“条件性磁共振兼容”器械,这些要求对患者的使用增加了新限制。若未遵照更新后的使用说明书,可能造成患者受伤。
采取措施:
DePuy Synthes于2014年7月4日再次发布了现场安全通告(FSN),该通告是对2014年4月14日第一次发布现场安全通告(FSN)的补充。通告要求相关单位及医护人员根据两次发布的通告说明识别受影响器械,下载或向制造商索要新版使用说明书副本,确保相关员工(特别是MR检测人员)知晓变更内容,返回制造商确认表,同时确保所有蚀刻有“MR-Safe(MR安全)”的DePuy Synthesy外固定产品被视为条件性磁共振兼容器械,并按照更新后的条件性磁共振兼容标签规定使用。
这些器械作为条件性磁共振兼容器械可以进入MR环境,但必须按下列要求进行放置:1、正常作业模式时,Synthes小型和大型外固定系统应放置于磁共振成像(MRI)孔外 ,Synthes中型和DO环型外固定系统放置于距离MRI孔外缘7cm以内;2、一级控制模式时,所有Synthes外固定系统完全位于MRI孔外。详细使用参阅产品使用说明书MRI说明部分。
附:MR标识术语解释:
MR Safe(MR安全)— 用于无传导性、非金属以及无磁性且在所有MR环境下均不会产生已知危害的产品,如塑料培养皿。
MR Conditional(条件性磁共振可兼容)— 用于已经证实在特定应用条件及MR环境下不会引产生已知危害的产品。确定MR环境的条件,包括静态磁场强度、射频场、比吸收率以及图像周围伪影失真。对于条件性磁共振可兼容产品,产品所贴标签上含有足以表征该产品在MR环境中表现的试验结果。
MR Unsafe(MR不安全) — 已知在所有MR环境下均会产生危害的产品,如铁剪刀。
(英国MHRA网站)











