![]() (ba) ad 将分离出的H2重新通入容器中,平衡正向移动,Se的转化率提高 550℃,0.3 MPa 碱性 c(Na+)=c(HSe)+c(Se2)+c(H2Se) CO2e+H2O=CO2+2H+ 1.6×1012
(ba) ad 将分离出的H2重新通入容器中,平衡正向移动,Se的转化率提高 550℃,0.3 MPa 碱性 c(Na+)=c(HSe)+c(Se2)+c(H2Se) CO2e+H2O=CO2+2H+ 1.6×1012
【解析】
(1)根据盖斯定律求出反应的H;
(2)①该反应为气体的总物质的量不变的反应,根据反应达到平衡的判断依据作答;
②分离出的H2重新通入反应容器,会增大反应物中H2的浓度,据此分析对平衡的影响效果;
③结合已知图像分析作答;
(3)HSe 在溶液中存在电离平衡和水解平衡,根据已知条件求出HSe的水解平衡常数,进而比较出水解程度与电离程度的相对大小分析,再结合物料守恒作答;
(4)通入CO的Pt电极为原电池的负极,依据原电池原理书写其电极反应式;
(5)根据沉淀转化的化学平衡常数与各沉淀溶度积之间的关系进行计算。
(1)根据盖斯定律可知ΔH3 =![]() (ΔH2ΔH1)=
(ΔH2ΔH1)=![]() (ba)kJ·mol1,
(ba)kJ·mol1,
故答案为![]() (ba);
(ba);
(2)①由于反应前后气体的质量发生了变化,但气体的总物质的量不变,则
a. 建立平衡过程中气体质量增加,容器体积不变,气体密度增大,达到平衡时气体质量不变、气体密度不变,气体的密度不变能说明反应达到平衡状态;
b. υ(H2)= υ(H2Se)没有指明反应速率的方向,υ(H2)= υ(H2Se)不能作为达到平衡的判定依据;
c. 反应过程中在任何时刻压强都不改变,所以压强不变不能作为反应达到平衡的判定依据;
d. 建立平衡过程中气体质量增加,气体物质的量不变,气体的平均摩尔质量增大,达到平衡时气体质量不变,气体的平均摩尔质量不变,气体的平均摩尔质量不变能说明反应达到平衡状态;
故答案为ad;
②将平衡混合气通入气体液化分离器气体H2Se转化为液体H2Se,并将分离出的H2重新通入反应容器,会增大反应物中H2的浓度,平衡正向移动,Se的转化率提高,
故答案为将分离出的H2重新通入容器中,平衡正向移动,Se的转化率提高;
③由于最终是以5小时内得到的H2Se为产量指标,则从图1可知,在550℃时产率最高,所以最适宜的反应温度为550 ℃;由图2可知,反应5小时左右时,压强为0.3 Mpa条件下产率最高,因此最适宜压强为0.3 Mpa,
故答案为550℃,0.3 MPa;
(3)HSe 在溶液中存在电离平衡和水解平衡,HSe的水解平衡常数 = ![]() ≈7.7×1011>K2=5.0×1011,即HSe的水解能力大于其电离能力,则NaHSe溶液呈碱性,溶液中的物料守恒关系为c(Na+)=c(HSe)+c(Se2)+c(H2Se),
≈7.7×1011>K2=5.0×1011,即HSe的水解能力大于其电离能力,则NaHSe溶液呈碱性,溶液中的物料守恒关系为c(Na+)=c(HSe)+c(Se2)+c(H2Se),
故答案为碱性;c(Na+)=c(HSe)+c(Se2)+c(H2Se);
(4)根据题意,结合装置图,石墨极上Se得到电子发生还原反应生成H2Se,则石墨为正极,Pt为负极,在Pt电极上CO失电子发生氧化反应,电极反应式为CO2e+H2O=CO2+2H+,
故答案为CO2e+H2O=CO2+2H+;
(5)反应CuS(s)+Se2(aq)![]() CuSe(s)+S2(aq)的化学平衡常数K=
CuSe(s)+S2(aq)的化学平衡常数K=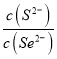 =
=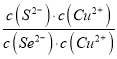 =
=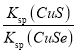 =
=![]() ≈1.6×1012,
≈1.6×1012,
故答案为1.6×1012。










