贵州医科大学附属医院超声中心主任,教授,主任医师,博士,硕士研究生、博士研究生导师
学术任职:
中华医学会超声医学分会常务委员,中华医学会超声介入专委会委员,中国超声医学工程学会浅表器官及外周血管专业委员会委员,贵州省医学会超声医学分会主任委员,贵州省超声工程学会副会长,贵州省超声医学质控中心主任。
上下滑动查看更多信息
医学博士,主治医师
主要研究方向:
超声分子影像学技术在心血管重构机制解析及肿瘤靶向治疗中的应用及相关机制
学术任职:
中国超声医学工程学会分子影像超声专业委员会青年委员;贵州省中华医学会超声医学分会青年委员。
上下滑动查看更多信息
-
作者
赵丽娜,黄丹,李晓怡,廖春雁,李莎,张蓓*
-
本文引用格式
[1]赵丽娜,黄丹,李晓怡,等.超微血流成像评估超声空化对4T1乳腺癌小鼠微血流灌注的影响[J].中国医学影像学杂志,2026,34(1): 22-28.DOI:10.3969/j.issn.1005-5185.2026.01.005.
-
目的
探究超微血流成像评估超声空化作用4T1乳腺癌小鼠后微血流灌注的影响。
-
资料与方法
构建4T1乳腺癌小鼠模型,随机分成对照组、超声空化组(连续辐照、间歇辐照)、微泡组、单纯辐照组,每组5只。经尾静脉注射自制超声微泡,超声探头对小鼠肿瘤辐照,微泡组仅注射微泡,单纯辐照组仅进行辐照不注射微泡,超声空化组共辐照5 min,分别为连续辐照或间歇辐照(辐照5 s、间歇5 s)。通过超声造影和微血流成像分别在超声空化前、超声空化后立刻、3 h、6 h、24 h评估小鼠肿瘤内血流灌注情况。通过免疫组化分析肿瘤组织中CD31表达水平。
-
结果
超声空化治疗前瘤体呈乏血供状态,空化后瘤体血流充盈较对照组提升约2倍,间歇辐照效果优于连续辐照(F=59.46,P<0.05),且与0 h比较,空化后3 h血供稍减少(t=9.31,P<0.05),6 h后作用效果减弱更加明显(t=11.42,P<0.05),至24 h后作用效果完全消失(t=16.37,P<0.05)。超微血流成像发现,与对照组对比,超声空化后肿瘤局部血流明显增加,随时间延长,血流量逐渐减少(P<0.05)。与对照组相比,空化后肿瘤血管密度无明显增加(F=1.839,P>0.05)。
-
结论
超微血流成像可以评估超声空化显著增加了4T1乳腺癌小鼠后微血流灌注,且随超声空化作用时间延长,血流逐渐减少。
乳腺癌是导致女性死亡率较高的恶性肿瘤,近年其发病率逐渐升高,发病年龄趋于年轻化[1]。由于乳腺癌异质性较高,临床亚型较多[2],不同组织病理分型与乳腺结构密切相关,且对患者预后和选择治疗方案尤为重要[3]。血管生成是乳腺癌的主要病理过程,与肿瘤发生、生长和侵袭有关,由缺氧的肿瘤微环境和多种促血管生成因子共同诱导。由于肿瘤内血流低灌注直接导致瘤体内部乏氧,不仅因内部环境偏酸性引起耐药,还可影响药物不均匀分布,从而促进肿瘤血管生成[4]。超声空化是一种新兴肿瘤治疗方式,可以通过改善肿瘤局部血流情况显著提高乳腺癌的治疗效果[5]。目前,超声评估病变血流的方式主要包括彩色多普勒血流成像(CDFI)、能量多普勒、超声造影(CEUS)、超微血流成像(ultra-micro angiography,UMA)以及超分辨显微造影,其中UMA是在非造影条件下提升低速微小血管血流显示的一种独特的实时非侵入性微血管成像多普勒技术[6]。本研究拟应用UMA、CEUS等观察乳腺癌小鼠瘤体内血流情况,评估超声空化后对瘤体内血流分布的影响,进一步探讨UMA是否可以作为评估乳腺癌宏观血流和微观血管密度的桥梁技术,为乳腺癌诊疗评估提供新方法。
1.1 主要试剂与仪器
二棕榈酰磷脂酰胆碱、二硬脂酰基磷脂酰乙醇胺-聚乙二醇2000(DSPE-PEG2000)(Avanti),VINNO G86诊断治疗一体机(苏州飞依诺科技有限公司),Resona A20(深圳迈瑞科技有限公司),组织摊片机[卓的仪器设备(上海)有限公司],青霉素/链霉素、含0.25% EDTA胰蛋白酶(北京索莱宝公司),胎牛血清(Biological Industries公司)、细胞快速冻存液(奕杉生物)、兔抗CD31(武汉三鹰生物科技有限公司),肌酐(creatinine,Cr)、尿素氮(urea nitrogen,BUN)、天冬氨酸氨基转移酶(aspartate aminotransferase,AST)、丙氨酸氨基转移酶(alanine aminotransferase,ALT)试剂盒(南京建成生物科技股份有限公司),光学显微镜(Olympus),小鼠乳腺癌4T1细胞株(中科院上海细胞库),多功能酶标仪(BioTek)。
1.2 微泡制备及表征测定
称取二棕榈酰磷脂酰胆碱5 mg、DSPE-PEG2000 2 mg,加入甘油50 μl、PBS 450 μl后65℃水浴30 min。高压充气后振荡1 min,获得乳白色混悬液后,加入0.5 ml PBS定容,即得到微泡,于4℃存储备用。
1.3 构建乳腺癌小鼠皮下植瘤模型
在37℃、5% CO2及常规湿度条件下培养4T1小鼠乳腺癌细胞,用含RPMI 1640、10%胎牛血清、1%青霉素链霉素双抗的细胞培养液,待细胞处于对数生长期时,用胰蛋白酶消化40 s,离心去上清后,用无血清培养基调整细胞数量至1×107/ml。选取25只BALB/c雌性小鼠(6周,18~20 g,贵州医科大学动物实验中心提供)。本实验经贵州医科大学实验动物伦理委员会批准(2101289),将0.1 ml细胞悬液接种至雌性小鼠右侧腹股沟皮下,取肿瘤最大径>1.0 cm且形态规则的瘤体,将小鼠根据体重编号随机分为5组,每组各5只,对照组(不进行任何干预)、微泡组(仅经尾静脉注射微泡)、连续辐照组(经尾静脉注射微泡后不间断用超声辐照肿瘤)、间歇辐照组(经尾静脉注射微泡后间断用超声辐照肿瘤)、单纯辐照组(仅用超声辐照肿瘤)。
1.4 超声空化治疗
按照实验分组进行超声空化治疗(VINNO G86诊断治疗一体机),对照组及微泡组不进行超声空化治疗,连续辐照组、间歇辐照组及微泡组经小鼠尾静脉注射稀释后的微泡(0.05 ml微泡混合于1 ml生理盐水中,微泡浓度为0.3 mg/ml),注射时间持续至辐照结束,随后对肿瘤区域进行超声辐照5 min,辐照时保证探头与肿瘤区域表皮良好耦合。治疗超声参数:最大声强688.93 mW/cm2,探头4-12 L,机械指数为0.2,脉冲宽度为5.5个周期,脉冲重复频率1 000 Hz,工作3 s、间歇3 s,总辐照时间5 min。
1.5 超声评估
各组分别行二维超声、CEUS、UMA等观察肿瘤。应用Resona A20诊断超声仪适度调节机器深度,焦点放置于瘤体中央,使用LM18-5Wu线阵探头,探头频率18~24 MHz。首先,在灰阶超声下观察瘤体形态、大小、内部回声等,并测量瘤体大小;CDFI模式下观察肿瘤内部及周边血流情况,调整增益动态观察瘤体内血流情况;随后进行UMA,激活UMA后将感兴趣区框置于目标病变区,调节感兴趣区框大小覆盖目标病变并包含适量比邻组织,避免感兴趣区框过大或过小,调节增益等参数,提高对低速血流灵敏度、减少运动伪影,切换3种不同子模式(cUMA:血流速度和方向;pUMA:血流能量和方向;sUMA:血流能量信息),并保存图像分析血流像素比。最后进行CEUS,先将自制微泡与生理盐水充分混合,调整仪器机械指数为0.08,经小鼠尾静脉注射约0.1 ml微泡(浓度为0.3 mg/ml),同时启动造影模式,动态存储视频30~60 s并进行定量分析。
1.6 HE染色及免疫组化染色
超声检查后以过量戊巴比妥钠处死小鼠,沿肿瘤包膜与正常组织边界完整剥离肿瘤组织,用生理盐水漂洗后固定于4%多聚甲醛中,石蜡包埋,制作5 μm组织切片,行HE染色和CD31免疫组化染色,筛选阳性染色最密集区,并随机计数3个视野内的微血管数,取平均值即为肿瘤微血管密度。
1.7 肝肾功能测定
根据试剂盒说明书步骤测定Cr、BUN、AST、ALT。
1.8 统计学方法
采用SPSS 23.0和GraphPad Prism 8.0.2软件,符合正态分布的计量资料以x±s表示。两组间比较采用t检验,多组间比较采用单因素方差分析,两两比较采用LSD法。P<0.05表示差异有统计学意义。
2.1 微泡制备及表征
成功制备的微泡为乳白色,光镜下大小均匀,分散性好(图1)。NanoBrook粒径仪测微泡粒径为(335.67±31.06)nm,Zeta电位为(-4.13± 1.30)mV。
图1 自制微泡。A为制备的微泡;B为光镜下微泡分布(×200)
2.2 4T1乳腺癌模型构建
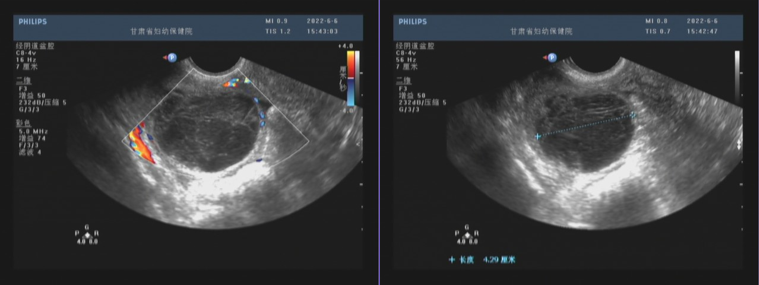
建模前后各组小鼠体重差异无统计学意义(F=0.30,P>0.05,图2A)。建模后第14天小鼠腹股沟区可见球形肿块,各组间肿瘤体积差异无统计学意义(F=1.56,P>0.05,图2B)。超声声像图显示一低回声球形团块,边界清晰,内回声尚均质,可见少许血流信号,各组瘤体大小差异无统计学意义(F=0.60,P>0.05,图2C、D)。
图2 二维超声小鼠瘤体图像。A. 4T1乳腺癌模型小鼠体重变化;B. 4T1乳腺癌模型小鼠瘤体体积变化;C、D. 4T1乳腺癌模型小鼠超声检测瘤体体积
2.3 不同模式超声空化后4T1乳腺癌瘤体血流灌注
4T1乳腺癌小鼠瘤体呈乏血供状态,CEUS显示瘤体呈高增强,向心性灌注,中央部分区域未见造影剂填充,在造影过程中部分瘤体内部无灌注,部分瘤体可见穿支血管、血管紊乱等现象。超声空化治疗后CEUS显示瘤体内血流充盈明显增多,尤其是间歇辐照组,连续辐照峰值强度约为对照组的2.2倍,间歇辐照约为对照组的2.6倍,差异有统计学意义(F=59.46,P<0.05)(图3A、E、F)。UMA主要检测到瘤体边缘或比较粗大的血管,与对照组相比,超声空化后瘤体内局部血流信号增加,半定量分析显示与对照组相比,超声空化后血流像素比明显增多(cUMA、pUMA、sUMA对应的F值分别为56.75、94.82、86.00,P均<0.05),尤其是间歇辐照组(图3B~D、G~I)。
图3 CEUS、UMA检测不同组别瘤体内血流灌注。A、E、F.小鼠瘤体CEUS图、造影灰度值和峰值强度;B、G.小鼠瘤体cUMA成像图及血流像素比;C、H.小鼠瘤体pUMA成像图及血流像素比;D、I.小鼠瘤体sUMA成像图及血流像素比。CEUS为超声造影,UMA为超微血流成像,aP<0.05,bP<0.001,cP<0.000 1
2.4 超声空化后不同时相4T1乳腺癌瘤体血流灌注
为进一步验证间歇超声辐照后瘤体内血流灌注动态变化,本研究分别于治疗后即刻、3 h、6 h及24 h采用CEUS及UMA评估瘤体内血流,结果显示间歇超声空化后肿瘤局部血流明显增加,随着时间延长,血流量逐渐减少(图4A~D)。CEUS峰值强度定量分析显示,与0 h相比,随着时间延长,瘤体内血流灌注持续减少,3 h血流信号降低约1.3倍(t=9.31,P<0.05),6 h降低50%以上(t=11.42,P<0.05),至24 h血流灌注与未空化相似,血流恢复至基础状态(t=16.37,P<0.05),3 h与6 h差异无统计学意义(t=2.11,P>0.05,图4E、F)。血流像素比结果与上述结果类似(cUMA、pUMA、sUMA对应的F值分别为37.25、50.29、35.82,均P<0.05,图4G~I)。
图4 CEUS、UMA检测超声空化后不同时间瘤体内血流灌注。A、E、F.小鼠瘤体不同时间超声造影图及造影灰度值和峰值强度;B、G.小鼠瘤体不同时间cUMA成像图及血流像素比;C、H.小鼠瘤体不同时间pUMA成像图及血流像素比;D、I.小鼠瘤体不同时间sUMA成像图及血流像素比。CEUS为超声造影,UMA为超微血流成像,aP<0.05,bP<0.001,cP<0.000 1
2.5 4T1乳腺癌瘤体血管密度
HE染色结果显示,各组间瘤体无显著差异。免疫组化检测瘤体CD31表达水平,结果显示与对照组相比,空化后肿瘤血管密度无明显增加,各组间差异无统计学意义(F=1.839,P>0.05),见图5。
图5 乳腺癌瘤体内血管密度(×200)。A. HE染色示肿瘤细胞大小各异、排列杂乱;B、C. CD31免疫组化染色,棕黄色越多,代表CD31表达含量越多
2.6 4T1乳腺癌小鼠肝肾功变化
为明确制备的微泡和超声空化对小鼠的影响,通过血生化检测肝肾功能,结果发现与对照组相比,各组间AST、ALT、Scr、BUN差异无统计学意义(F=0.28、0.01、0.41、0.10, P均>0.05),见表1。
乳腺癌是女性常见恶性肿瘤之一,血管生成与肿瘤进展密切相关。精准显示肿瘤的血供不仅可以鉴别良恶性,还可以评估增加血供对临床疗效的影响[7]。本研究通过UMA和CEUS精准、可视化评估超声空化后,小鼠瘤体内血流灌注显著增加,内部乏血供区域血流显示增多,血流分布不仅局限于边缘,中央区也可以显示血流灌注,并且在超声空化作用6 h后血流逐渐减少。
3.1 UMA、CEUS可视化评估瘤体内血流灌注的影响
肿瘤内血管特征可以作为评估肿瘤性质的依据,CDFI、UMA、CEUS均是超声评估肿瘤内血流的影像学检测方法[8]。本研究发现,UMA较CDFI更好地显示小鼠瘤体内血流,通过半定量血流像素比分析瘤体内血流占比发现超声空化后可显示的血流占比明显增多。与既往研究一致,血流指数可以评估肿块内血流密度[9],恶性病变的UMA血流信号分级高于良性病变[10]。CEUS可以实时、动态、持续评估乳腺病灶增强速度与强度、肿瘤内造影剂分布特征[11],能够预测肿瘤性质、病理学分级、转移等[12-13]。恶性肿瘤呈不均匀高增强,血管扭曲、紊乱,血流灌注可有缺损区域[14-15],与本研究一致,乳腺癌小鼠瘤体呈不均匀高增强,中央区未见血流灌注,这可能是因为恶性肿瘤生长迅速,血管排列紊乱,内部血流供应差,导致局部出现缺血坏死[16]。肿块CEUS强化特征和定量参数峰值强度及曲线下面积的变化可以预测乳腺癌病理分型及新辅助化疗后患者病理学完全缓解[17]。本研究中超声空化后峰值强度明显增高,表明超声空化后增加了局部组织灌注量及血管密度。
3.2 超声空化增加瘤体内血流灌注
恶性肿瘤血流由周边向内部快速提供营养,部分肿瘤中间因乏氧乏血供导致疗效不佳[18],肿块内血流丰富可以提高临床长期疗效[7]。针对乏血供肿瘤可以通过超声空化增强瘤体内部血流灌注,低强度、短时间、频率高的血流灌注效果更好。与既往研究类似,低声压、低机械指数治疗可刺激肿瘤血流灌注增加[19],而高声压、高机械指数治疗对动物肿瘤微血管可以产生损毁效应,主要是扩张肿瘤微血管、管壁结构崩解,弥漫性出血、组织水肿和局部血肿血栓形成,毁损并阻断肿瘤循环[20]。本研究发现,空化后瘤体血流明显增多,3 h逐渐减少,24 h则恢复空化前的血流状态。这可能是因为超声空化刺激瘤体导致瘤体内血管扩展,血管内皮发生短暂可复损伤。此外,超声空化可以诱导血管正常化而抑制胰腺癌生长和转移[21]。超声空化靶向治疗可以重建肿瘤微环境,改善免疫治疗效果,抑制上皮间充质转换进程[22-24]。这些研究表明超声空化可以通过调控瘤体内血流灌注,低强度、短时间、频率高的血流灌注更明显,提高肿瘤局部药物浓度和疗效。
UMA和CEUS定量参数与微血管密度相关[25],但本研究中超声空化治疗前后瘤体血管密度未发生明显变化,可能是因为超声空化短暂的刺激未促进血管新生,而是以增加血管内血流量为主,肿瘤内新生小血管较多,超声空化开放了更加细微的小血管,促使造影剂通过更多微小血管。超声空化前后小鼠肝肾功能、体重等未发生明显变化,进一步表明超声空化刺激对乳腺癌小鼠未造成显著损伤,表明其生物安全性好。
3.3 不足与展望
本研究验证了UMA和CUES可以评估超声空化治疗可立即增强肿瘤内血流灌注,间歇刺激的血流灌注效果较好,且随超声空化作用时间延长,血流逐渐减少,证实UMA可以作为评估超声空化刺激后乳腺癌微循环的新方法,为乳腺癌诊疗提供基础实验支持。然而,本实验未进一步比较在多次、长期治疗过程中,超声空化治疗不同参数和条件组合对肿瘤血流灌注的影响,后续将进一步深入探索超声空化增强肿瘤血流灌注的条件和具体机制。
利益冲突 所有作者均声明不存在利益冲突
[1] Siegel RL, Kratzer TB, Giaquinto AN, et al. Cancer statistics, 2025[J]. CA A Cancer J Clin, 2025, 75(1): 10-45. DOI: 10.3322/caac.21871.
[2] Han B, Zheng R, Zeng H, et al. Cancer incidence and mortality in China, 2022[J]. J Natl Cancer Cent, 2024, 4(1): 47-53. DOI: 10.1016/j.jncc.2024.01.006.
[3] Nolan E, Lindeman GJ, Visvader JE. Deciphering breast cancer: from biology to the clinic[J]. Cell, 2023, 186(8): 1708-1728. DOI: 10.1016/j.cell.2023.01.040.
[4] Wu T, Lucas E, Zhao F, et al. Artificial intelligence strengthens cervical cancer screening – present and future[J]. Cancer Biol Med, 2024, 21(10): 864-879. DOI: 10.20892/ j.issn.2095-3941.2024.0198.
[5] Wang H, Liu Y, Li Y, et al. Ultrasound-responsive drug delivery system for cancer therapy[J]. Macromol Biosci, 2025, 25(11): e00082. DOI: 10.1002/mabi.202500082.
[6] Feng J, Lu J, Jin C, et al. Diagnostic value of superb microvascular imaging in differentiating benign and malignant breast tumors: a systematic review and meta-analysis[J]. Diagnostics, 2022, 12(11): 2648. DOI: 10.3390/ diagnostics12112648.
[7] 刘育彤. 超声超微血流成像评估乳腺癌新辅助化疗疗效的研究[D]. 广州: 广州医科大学, 2023.
[8] 王莉, 胡兵, 任亮, 等. 多种超声影像技术在乳腺癌诊断中的研究进展[J]. 中国医学影像学杂志, 2024, 32(6): 635-640. DOI: 10.3969/j.issn.1005-5185.2024.06.021.
[9] Chae EY, Yoon GY, Cha JH, et al. Added value of the vascular index on superb microvascular imaging for the evaluation of breast masses: comparison with grayscale ultrasound[J]. J Ultrasound Med, 2021, 40(4): 715-723. DOI: 10.1002/jum.15441.
[10] 韩敏, 张宇, 路红, 等. 剪切波弹性成像和超微血管成像辨别乳腺早期恶性病变的价值[J]. 郑州大学学报(医学版), 2022, 57(3): 357-361. DOI: 10.13705/j.issn.1671-6825. 2021.10.025.
[11] Wen B, Kong W, Zhang Y, et al. Association between contrast-enhanced ultrasound characteristics and molecular subtypes of breast cancer[J]. J Ultrasound Med, 2022, 41(8): 2019-2031. DOI: 10.1002/jum.15886.
[12] 杨雁雯, 李伟伟, 陶玲玲, 等. 小乳腺癌的超声造影特征与病理组织学分级的相关性研究[J]. 中国医学计算机成像杂志, 2024, 30(5): 594-598. DOI: 10.19627/j.cnki.cn31-1700/th.2024.05.008.
[13] 郭振宁, 郝振民, 邓宇光. 超微血管成像联合剪切波弹性成像在老年女性乳腺癌中的应用价值[J]. 中国老年学杂志, 2023, 43(19): 4649-4652. DOI: 10.3969/j.issn.1005-9202.2023.19.012.
[14] Lee SC, Tchelepi H, Khadem N, et al. Imaging of benign and malignant breast lesions using contrast-enhanced ultrasound: a pictorial essay[J]. Ultrasound Q, 2022, 38(1): 2-12. DOI: 10.1097/RUQ.0000000000000574.
[15] Wang X, He Y, Wang L. Diagnostic value of shear wave elastography combined with super microvascular imaging for BI-RADS 3-5 nodules[J]. Front Oncol, 2023, 13: 1192630. DOI: 10.3389/fonc.2023.1192630.
[16] Arner EN, Rathmell JC. Metabolic programming and immune suppression in the tumor microenvironment[J]. Cancer Cell, 2023, 41(3): 421-433. DOI: 10.1016/j.ccell.2023.01.009.
[17] 胡高杰, 张小杉, 樊炳慧, 等. 超声造影在不同分子分型乳腺癌鉴别诊断中的应用[J]. 中国医学影像学杂志, 2024, 32(11): 1134-1139. DOI: 10.3969/j.issn.1005-5185. 2024.11.008.
[18] Luo R, Wang Q, Zhang Y, et al. Value of contrast-enhanced microflow imaging in diagnosis of breast masses in comparison with contrast-enhanced ultrasound[J]. Acad Radiol, 2024, 31(6): 2217-2227. DOI: 10.1016/j.acra.2023.11.021.
[19] Wu N, Cao Y, Liu Y, et al. Low-intensity focused ultrasound targeted microbubble destruction reduces tumor blood supply and sensitizes anti-PD-L1 immunotherapy[J]. Front Bioeng Biotechnol, 2023, 11: 1173381. DOI: 10.3389/fbioe. 2023.1173381.
[20] Hong D, Yang J, Guo J, et al. Ultrasound-targeted microbubble destruction enhances inhibitory effect of apatinib on angiogenesis in triple negative breast carcinoma xenografts[J]. Anal Cell Pathol, 2021, 2021: 8837950. DOI: 10.1155/ 2021/8837950.
[21] Lin L, Du Y, Hao J, et al. UTMD inhibits pancreatic cancer growth and metastasis by inducing macrophage polarization and vessel normalization[J]. Biomed Pharmacother, 2023, 160: 114322. DOI: 10.1016/j.biopha.2023.114322.
[22] Maardalen M, Carlisle R, Coussios C. Cavitation-mediated immunomodulation and its use with checkpoint inhibitors[J]. Pharmaceutics, 2023, 15(8): 2110. DOI: 10.3390/pharmaceutics 15082110.
[23] Liu S, Zhang Y, Liu Y, et al. Ultrasound-targeted microbubble destruction remodels tumour microenvironment to improve immunotherapeutic effect[J]. Br J Cancer, 2023, 128(5): 715-725. DOI: 10.1038/s41416-022-02076-y.
[24] Xu J, Wang Y, Li Z, et al. Ultrasound-targeted microbubble destruction (UTMD) combined with liposome increases the effectiveness of suppressing proliferation, migration, invasion, and epithelial- mesenchymal transition (EMT) via targeting metadherin (MTDH) by ShRNA[J]. Med Sci Monit, 2019, 25: 2640-2648. DOI: 10.12659/MSM.912955.
[25] Arthur LJMB, Voulgaridou V, Butler MB, et al. Comparison of contrast-enhanced ultrasound imaging (CEUS) and super-resolution ultrasound (SRU) for the quantification of ischaemia flow redistribution: a theoretical study[J]. Phys Med Biol, 2024, 69(23): 235006. DOI: 10.1088/1361-6560/ ad9231.
向下滑动查看更多参考文献
本文为《中国医学影像学杂志》原创文章。若您需要转载本文,请通过公众号联系本刊编辑部获得授权,并在醒目位置注明“原文刊发于《中国医学影像学杂志》,卷(期):起止页码”,期待与您的合作!
杂志微信公众号 | zgyxyxx
本刊官网 | http://zyyz.cbpt.cnki.net
编辑部电话 | 010-64012981转5200;15110102619