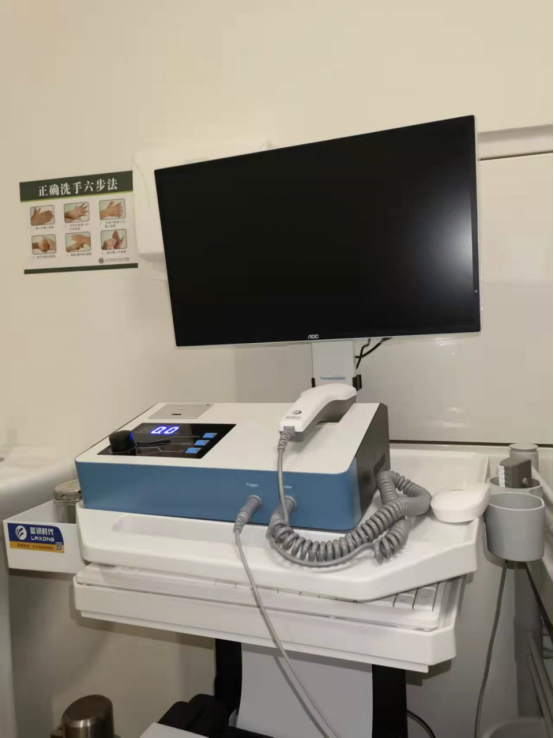
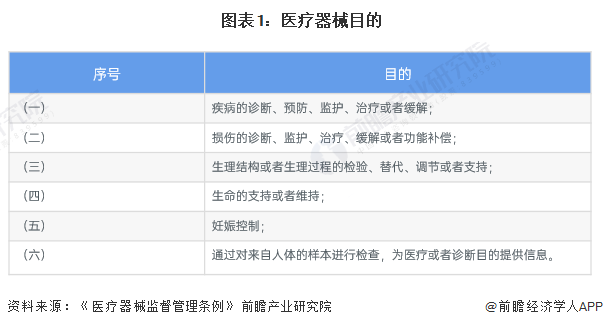
11月13日,湖北省药品监督管理局检查组一行莅临我中心,对已备案的医疗器械临床试验机构进行了全面、细致的日常监督检查,检查组在充分肯定的同时,也指出了需要完善之处。
自独立运行以来,市临床检验中心始终以提升专业技术能力为核心,不断精进检测水平,积极拓展业务服务范围,实现了从基础检验向科研创新与临床服务并重的转型发展。2023年,中心备案了临床化学、血液体液学、细胞分子遗传学三个医疗器械临床试验专业。以此为契机,中心将医疗器械临床试验作为提升机构综合实力、服务医疗器械产业创新发展的重要抓手,通过构建完善的质量管理体系,培养专业人才队伍,为医疗器械的科学评价与产业升级提供坚实的技术支撑,开展了Leber遗传性视神经病变基因检测试剂盒(PCR-荧光探针法)和Avellino角膜营养不良基因检测试剂盒(PCR-荧光探针法)2项临床试验。
现场检查持续了数小时,专家组通过听取汇报、现场考察、文件审查和记录追溯等多种方式,对中心的医疗器械临床试验质量管理体系进行了系统性评估。机构办公室就本中心临床试验管理部门架构、人员配置、管理制度、标准操作规程以及自备案以来承接的2项GCP项目的运行情况,向专家组作了详细汇报。随后,专家组对实验室现场的试验环境条件、仪器设备校准与维护、样本管理流程等进行了严格核查,并重点检查了质量管理体系文件、人员培训档案、两项在研项目的伦理批件、试验方案、原始记录及严重不良事件(SAE)处理流程等。检查过程紧张有序,专家组对中心在短时间内构建起较为完善的医疗器械临床试验质量管理体系,并成功运行项目给予了积极评价,同时也指出了需要完善之处。
此次检查为中心医疗器械临床试验工作的规范化建设指明了具体方向。中心将以此为契机,秉持“科学、规范、诚信、创新”的原则,将检查成果以及后续的整改过程转化为持续发展的动力。下一步,我们将进一步细化完善制度及质量体系文件,并重点深化人员培训、完善流程细节、积极拓展合作,力争在已备案领域承接更多具有影响力的临床试验项目,不断提升核心竞争力。