11.将废旧锌锰电池处理得到含锰混合物,既能减少它对环境的污染,又能实现废电池的资源化利用.
Ⅰ.回收二氯化锰:将废旧锌锰电很处理,得到含锰混合物,向该混合物加入浓盐酸并加热.
(1)写出MnO(OH)与浓盐酸反应的化学方程式:2MnO(OH)+6HCl $frac{縛line{;;△;;}}{;}$2MnCl2+Cl2↑+4H2O.
II.锰回收新方法:向含锰混合物加入一定量的稀硫酸、稀草酸,并不断搅拌至无气泡为止,其主要反应为:2MnOOH+MnO2+2H2C2O4+3H2SO4=3MnSO4+4CO2↑+6H2O
(2)与使用浓盐酸回收锰相比,新方法的优点是工艺流程简单;生成CO2和H2O不影响MnSO4纯度;反应过程无有毒有害物质生成,不造成二次污染;废物资源化等(答1点即可).
(3)欲以MnSO4溶液为原料制备MnCO3,选用的加料方式C(填字母),原因是避免先生成Mn(OH)2. 己知:Ksp(MnCO3)=2.3×10-11、Ksp[Mn(OH)2]=2.l×10-13
A.将MnSO4溶液与Na2CO3溶液同时加入到反应容器中
B.将MnSO4溶液缓慢加入到盛有Na2CO3溶掖的反应容器中
C.将Na2CO3溶液缓慢加入到盛有MnSO4溶液的反应容器中
D.以上三种方式都无法得到MnCO3
III.现以含锰混合物为原料制备锰锌铁氧体的主耍流程如图l 所示: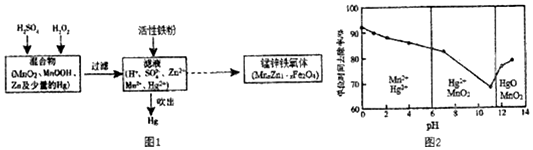
回答下列问题:
(4)MnxZn1-xFe2O4中铁元素化合价为+3,则锰元素的化合价为+2.
(5)活性铁粉除汞时,铁粉的作用是还原剂 (填“氧化剂”或“还原剂”).
(6)酸浸时,MnO2与H2SO4、H2O2反应的离子方程式为MnO2+H2O2 +2H+=Mn2++O2↑+2H2O.
(7)除汞是以氮气为载气吹入滤液中,带出汞蒸气经KMnO4溶液进行吸收而实现的.在恒温下不同pH时,KMnO4溶液对飞的单位时间去除率及主要产物如图2 所示:
①写出pH=10时KMnO4溶液吸收汞蒸气的离子方程式5Hg+2MnO4–+16H+═2Mn2++5Hg2++8H2O.
②在强酸性环境中汞的单位时间去除率高,其原因除氢离子浓度增大使KMnO4溶液的氧化性增强外,还可能是Mn2+对反应起催化作用,单位时间内去除率高.