产品开发意味着创造具有新特性或不同特性的产品,以满足不同的客户需求或提升现有客户的满意度[1]。在此过程中,信息从需求、要求和限制转化为能够满足这些需求的物理结构[2]。从总体角度来看,产品开发是“要实现什么”与“如何实现”之间的相互作用[3]。
聚焦于医疗器械,产品开发比传统产品的开发更为困难。基本上,在医疗领域,这类产品必须遵循并克服大量的法规、标准、程序和控制措施。在进入市场之前,设计人员必须确保产品的完全安全——既要满足与产品相关的所有要求,又要保证制造过程以及质量控制程序的安全性和有效性[1]。各国的法规各不相同,所有在某个国家销售的医疗器械都必须符合当地的法规。这些法规保护消费者的健康和安全性,导致开发过程变得更加严格。
医疗器械产品开发领域面临着诸多机遇,但也存在一系列挑战[4]。在工艺开发的多个方面,药物或设备领域的竞争日益激烈,这是一个突出的挑战。医疗器械公司必须具备柔韧性和创新性,以确保在市场上取得成功、保证客户满意度,并满足这一高度监管和控制的行业的所有要求[4]。降低产品成本、缩短产品开发时间、改进的功能以及可靠且高质量的产品以实现更高的客户满意度,在该领域正变得越来越重要。不断增加的产品复杂性和多种医疗器械的微型化趋势,导致设计出具有复杂几何形状和严格公差的小型部件,这对制造技术和自动化技术产生了重大影响。此外,产品需要满足大量功能,这意味着必须使用更先进的组件,并推动新型生物相容性材料的开发,以实现高水平的性能[4]。
开发医疗器械所需的投资相当高,有时设备的生命周期和批量大小不足以收回这些投资[5]。此外,众所周知,许多产品在初期测试中未能满足规格要求,因此可能需要追加投资。
在医疗器械行业,存在大量用户,他们使用设备的方式不同,期望各异,并且对设备有着独特的看法。通常,中间或最终用户并不直接负责设备或治疗的支付。区分客户和用户[1]这两个术语非常重要。客户可定义为购买商品或服务但不一定从中受益的个人或公司,可能是政府、企业或工程师。用户是指使用医疗器械用于自身或他人治疗和/或护理的人员,可能包括医疗专业人员、患者、护理人员或有特殊需求的人群等[1]。为了确保最终产品的成功,在医疗器械的开发过程中必须同时考虑用户和客户的需求。
2.1.1 生物医学产品生命周期
与传统产品相比,生物医学产品的生命周期更长,尽管在开发过程中需要考虑更多问题。图2.1展示了器械与放射健康中心和美国FDA 2011[6]医疗器械产品生命周期各阶段的循环模型。与传统产品类似,这些阶段从概念创建开始,到退出结束,涉及设计、制造过程规划、质量控制、生产管理、维护、售后服务以及上市后监测等学科。然而,对于生物医学产品而言,在开始制造过程之前,必须进行原型开发、临床前研究和临床分析,以实现测试、改进、再测试、验证、优化和定型。由于严格的验证要求,其过程更为复杂。
)
医疗器械产品开发的进展并非以线性方式进行,而是通过反馈循环以及不同阶段之间的重叠来推进。基本上,在早期阶段会开发出原型;随后通过一系列关于毒性、生物相容性和安全性的临床前测试对设计进行确认,从而导致对所创建设备的多次重新设计和调整。接下来,借助改进后的设计,临床试验能够更准确地分析这些问题,进一步推动重新设计以确保产品的安全性与可靠性;然后这些测试结果必须通过监管机制,符合各国监管机构所规定的要求。有时,即使产品已进入市场,产品评估和修改仍会继续进行[6]。
从更侧重于产品设计的工程视角来看,El‐Haik和Mekki[7]提出了如图2.2所示的线性生命周期模型。该生命周期从创意到处置共分为10个阶段。
第一至第五阶段与开发传统产品所采用的阶段类似。实际上,每个阶段都可以应用更多传统工具。首先,通过研发构思、基准测试、技术路线图和/或多代计划等技术产生创意。其次,确定设备拟销售国家的客户和监管机构提出的关键功能需求及所有约束条件,同时识别与产品接触的所有相关人员(利益相关者)。此阶段可采用质量功能展开(QFD)、公理化设计或功能分析。第三,提出多个
提出概念。在此阶段,可以使用TRIZ理论(又称发明问题解决理论)和形态矩阵来生成概念,而Pugh选择矩阵有助于从中选出最佳概念。在第四阶段,定义了大多数满足功能需求和约束条件的设计参数,从而形成设计结构。最终设计通过明确所有细节,并采用面向X的设计(DFX)、失效模式与影响分析(FMEA)以及制造工艺选择(MPS)等技术,确保设计无法以非预期的方式被使用,保证可制造性,并在产品进入市场前发现任何可能的错误。
详细设计的结果是生成原型样机。
从第6阶段开始,这些流程在医疗器械开发中变得更加具体。在第6阶段,制定验证与确认程序,并制造出原型。原型经过充分测试,进而进行最终调整以确保产品符合所有利益相关者的 要求 和 约束条件。接下来,在启动阶段,将评估所有 生产基础设施 和其他资源。在此阶段,需记录并确定 标准操作规程、人员的 培训程序 以及其他所需的特殊措施。在 生产阶段,制造工艺 应能够无缺陷地进行 制造,满足 第6阶段 所确定的所有 质量要求。本阶段使用的质量 方法包括 统计过程控制、田口方法、稳健设计、生产故障排除 和 诊断方法。最后,在最后两个阶段,产品被使用、退役并最终淘汰。适当的 售后服务 将通过修复 缺陷单元 和延长其 生命周期 来帮助保持 设计 的持续使用。
2.1.2 医疗设备开发过程
众所周知,有效的新产品开发(NPD)极大地影响着产品在市场上的成功可能性[8]。因此,在开发这些新产品时,整合文献中现有的产品开发模型非常重要。
一般来说,这些模型规定了为确保最终设计成功而需遵循的一系列活动,通过确保正确的人在正确的时间使用正确的信息来控制信息流,并且还详细说明了所采用的技术集合,以保证决策尽可能恰当。此外,众所周知,采用产品开发流程(PDP)的标准化模型可以缩短开发时间并降低最终产品成本。在这方面,医疗器械行业并无不同[1]。
在文献中,已提出多个医疗器械开发的模型。2009年,皮策施等人[9]提出了专门针对医疗器械开发的从概念到商业化的阶段‐门控流程(图2.3)。该模型基于对积极参与医疗器械开发、法规和使用方面的专家进行的深入访谈而建立。阶段‐门控流程包括以下五个阶段:(1)启动——机会与风险分析,(2)方案制定——概念和可行性,(3)设计和开发——验证与确认,(4)最终验证——产品上市准备,以及(5)产品上市和上市后评估。在每个阶段中,针对与产品相关的各个功能组定义了必要的活动。由于该流程的复杂性,舒卢扎斯和皮策施详细阐述了各阶段与活动之间的相互关系[10]。
2013年,梅迪纳等人[8]开发了一个通用模型,该模型整合了产品开发、法规、标准化和专利申请。该模型根据信息类型分为五个集群,分别是产品开发与引入过程、医疗规格、美国FDA、标准和专利。每个集群的主要活动和关系都进行了详细说明。
2012年,达斯和阿尔莫诺尔[11]提出了一种基于并行工程方法的属性驱动并行工程(ADCE)流程,用于医疗器械开发。该模型以简化的流程图方式识别了生物医学产品开发中的主要活动。此外,它还提出了
在制定属性驱动规范(ADS)时,需考虑多种类型的知识,如工程、医疗、市场营销、质量、法规问题和制造。提出了三种类型的属性:客户、功能、法规,这些属性必须被记录并量化。此外,还提出了ADS驱动的设计控制,以确保满足各项要求。
Neelamkavil等人[12]开发了一种方法论,旨在实现医疗器械开发过程中所有信息的可追溯性——从客户需求到制造和测试。该方法论旨在帮助用户在产品开发的各个阶段捕获、管理和重用工程知识。
2.1.3 医疗器械的设计过程
医疗器械设计流程涉及工程、商业和医疗领域的问题,并整合了政府监管(国内和国际)以及认证机构的相关事项。为了确保医疗产品的安全性和有效性,已采用设计控制措施,该措施提供了一种系统化程序,用于在产品开发的不同阶段评估设计过程。根据Gilman等人[13],的说法,设计控制是在设计过程中需遵循的一套系统化程序,以确保最终产品安全、有效,并能在竞争性市场中取得成功。
生物医学产品的设计过程与传统产品设计经历相同的阶段:概念、开发、制造和分销。然而,在产品开发阶段必须定义验证测试计划,并在制造阶段实施产品确认测试计划[13]。
确认 和 验证 是广泛使用的术语,其定义因监管机构的不同而有所差异。根据亚历山大[14]和亚历山大和毕晓普[15]的观点:“确认关注的是设计相对于系统应实现的初始创意的一致性和完整性,而验证关注的是在设计和实施过程中,每个相态的输出是否满足前一个相态输出中规定的要求。” 为了明确官方定义,美国FDA在其题为医疗器械制造商设计控制指南 的文件中提供了瀑布模型,该模型给出了更实用的确认与验证框架(图2.4)。
瀑布模型表明,验证可确保设计输入中规定的要求在设计输出中得以满足,并意味着在产品开发的各个阶段对设计的若干问题进行详细审查。确认比验证更为复杂。设计验证是包括设计验证在内的所有工作的累积总和,并延伸至评估按照设计生产的设备是否真正满足用户需求和预期用途。
亚历山大和毕晓普[15]关于验证与确认的观点非常有趣,他们通过回答以下问题来理解这些概念:
- 验证:我们是否正在正确地构建产品?
- 确认:我们是否构建了正确的东西?
鉴于确认的复杂性和广泛性,亚历山大[14]提出了一种实用的方法,旨在使设备的确认过程更简便且经济。该方法通过一个设计用于确认的模型(DFV‐V模型)进行组织,该模型展示了将用户需求转化为物理医疗器械的主要步骤。这些步骤包括“设备设计”、“过程设计”和“生产开发”,每个步骤

设备用户需求 设计验证
过程验证 过程设计
开发生产 确认生产
医疗器械 图2.5 根据亚历山大和毕晓普的验证设计模型架构(DFV‐V模型)[15]。
与通过验证要求进行的确认和验证的相应程序相关(图2.5)。
本节介绍了医疗产品开发过程在两个案例研究中的应用:舟月骨假体和气管支架。在这两个案例中,均已制造出初步原型,但尚未进行临床前测试。每个案例均应用了多种传统设计技术。
2.2.1 舟月骨间韧带
舟月骨不稳可导致严重疼痛、肿胀以及活动受限,通常是由于一条或多条腕骨间韧带断裂所致,其中舟月骨间韧带(SLIL)最常受累。目前已有多种手术方法被推荐用于治疗SLIL慢性撕裂,包括舟状骨‐大多角骨‐小多角骨融合、舟状骨‐头状骨融合、关节囊固定术、背侧关节囊固定韧带修复、肌腱固定术以及骨‐韧带‐骨重建[19]。然而,这些技术大多数需要开放手术,可能导致较长的恢复时间、明显瘢痕,以及经常出现的腕关节僵硬[20]。
关节镜检查通常作为一种微创技术,用于准确检测和诊断腕韧带撕裂,并可在静态和动态性不稳定条件下直接观察内在和外在腕韧带。针对关节镜手术,结合关节镜技术和假体可能是处理该问题的良好解决方案[21, 22]。
一种用于替代SLIL功能的新型假体被设计并制造。该设计过程由腕关节镜领域的专家外科医生进行评估,所制造的原型使外科医生能够分析所采用方案的优缺点。通过应用正式方法获得的知识
设计方法以及该知识在产品开发不同阶段的可追溯性,使得新开发、设计过程控制和确认变得更加容易。
用于设计假体的方法论基于Phal等人提出的系统化设计方法,这是设计传统产品中最常见的程序之一。图2.6展示了为获取产品设计和原型所进行的各项活动。在设计过程中,首先提出主要的设计概念,并与专家医生进行评估,进而确定最终方案并加以优化。接着,在具体化设计阶段对形状和几何结构进行细化,并选定材料和初步制造工艺。最后,在详细设计阶段完成了图纸。
为了开发原型,首先选择了假体的最终制造工艺,然后设计并制造了工具和夹具,最后生产出了假体的第一个原型。
2.2.2 概念设计
解决SLIL不稳定的方案通过三种不同方法进行了研究:(1)科学研究,(2)基准测试,以及(3)专利分析。科学研究趋势可分为以下几类:(1)植入物分析,(2)针对腕关节相关问题的假体设计,(3)腕关节行为关于腕关节的运动和受力,(4)手术程序,以及(5)应用于医疗器械的设计方法论。在这些各个领域中,研究了最具相关性的论文,以获取所有可能影响假体设计的知识。关于市场基准测试,目前存在多种类型的腕关节植入物。其中一类用于替换腕部多块骨骼,另一类用于完全替代腕关节( E‐MOTIONTM 全腕系统、MaestroTM 全腕系统或BiaxTM 全腕系统),还有其他植入物旨在固定特定骨骼的微小骨块(HerbertTM 骨螺钉和 HCS 2.4/3.0 螺钉)。现有三项可用于修复或替换SLIL的专利: US0306480A1[24], US0177291A1[25],和US0076504A1[26]。
产品的功能分析可用于捕获产品必须满足的所有功能。如图2.7所示,必须展开层次分析中的至少三个层级,以整合假体所需完成的全部功能。功能分析中的每一项功能都必须通过与其相关联的功能需求(FRs)和约束( Cs)进行形式化表达[27]。功能需求(FR)表示产品必须实现的功能,且该描述独立于任何可能的解决方案[23],并由功能和限定条件[27]定义;

表2.1 新型假体功能需求(FRs)与设计约束(Cs)的识别
参见表2.1。限定条件限制了可能的设计方案,并由约束(Cs)表示。约束有两种类型[27]:功能约束和设计约束(表2.1)。功能约束直接限制功能或动作,例如舟骨与月骨可分离的距离范围(表2.1中的FR12)。设计约束是与部件的物理定义直接相关的限制(例如Cs2中定义的假体最大尺寸),或来自动作执行条件的限制(例如Cs1中规定的相容性材料性能)。每个FR必须至少定义一个功能约束,且每个FR可受多个设计约束[27]限制。
用于量化功能需求和约束条件的信息来自不同来源。例如,与载荷和运动相关的量化符(FR21 和 FR31)来自科学文献,而与解剖学或手术过程相关的量化符则来自医生的专业知识(FR11、FR12、Cs2、Cs6 或 Cs7)。当定量值不可获得时,功能需求无法被测量或验证,因此难以判断其是否得到满足。
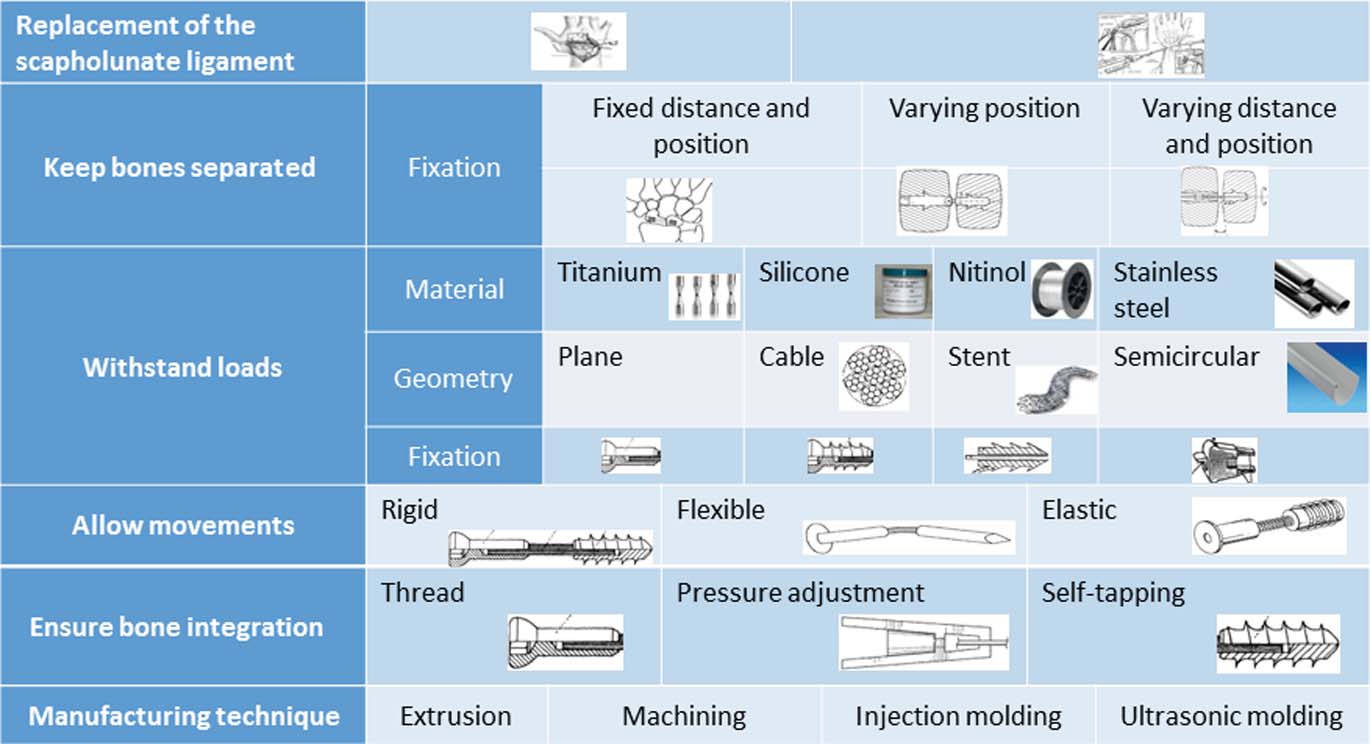
根据功能分析中的功能,建立了一个形态矩阵以生成可能的解决方案。因此,针对功能分析中的每一项功能,识别出了可能的物理解决方案。图 2.8展示了结果的综合。
不同物理解决方案的组合形成了三个主要设计概念:紧凑型系统(概念1) 和球窝‐球系统(概念2)。
概念1
概念2
概念3

)
以及导线系统;参见图2.9。紧凑型系统由于材料弹性特性,可调节两块骨骼之间的位置和距离,且通过圆头端实现骨整合。球窝‐球系统仅允许改变位置,而保持距离固定;其几何形状变化较多,与骨骼的整合通过压配系统实现。导线系统是柔韧性非常好,因为两个方向相反的编织导线能够恢复到初始位置。医生选择紧凑型系统的三个主要原因是:(1)由于材料的弹性,运动受限较少;(2)更易于插入和取出;(3)这是解决该问题的一个新颖的想法。从工程角度而言,第一个概念包含的部件更少,因此制造过程将更容易管理。
2.2.3 具体化设计
该紧凑型系统分为三个不同的部件:舟骨部分(刚性)、月骨部分(刚性)和弹性部分。
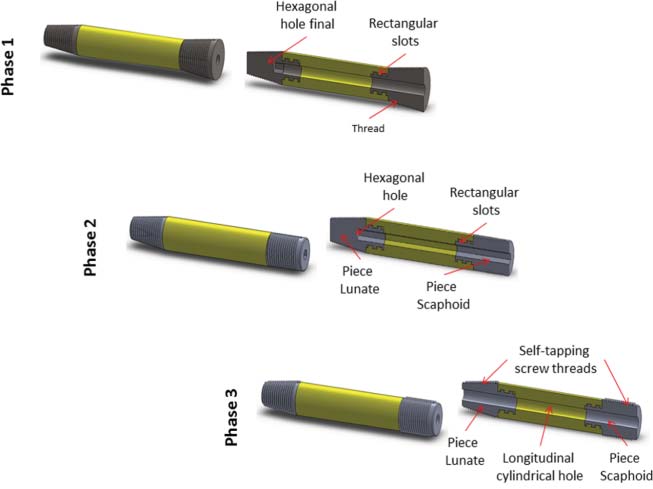
医生的知识使其能够在三个不同阶段进行优化,如图2.10所示。首先,中间关节被移至设备的末端,因为该连接可能损伤骨骼。末端改为带有轻微锥度的圆柱形,并增加了螺纹以增强骨固定和整合效果。刚性部分与弹性部分之间的连接通过矩形槽进行成型,以加强它们之间的固定。在假体内部引入了一个孔,该孔具有六角端,用于在将假体植入骨骼时传递旋转运动。其次,舟骨的锥形结构被改为圆柱形,因为这已足以确保装配的稳固性
骨头。假体内部孔为完全六角形,以在手术过程中插入假体时提高扭矩传递效率。最后,刚性端采用了自攻螺钉螺纹。使用克氏针(1mm直径)在假体上创建一个圆形孔,用于手术过程中引导设备。最后,还调整了一些关键尺寸,例如直径和长度。
2.2.4 详细设计
最终设计经过优化,以获得包含所有尺寸、材料和制造细节的最终图纸。假体长度小于20毫米,最大直径为3毫米(图2.11a)。刚性部件选用生物相容性钛,而弹性部分则选用生物相容性液态硅橡胶(LSR)。最后,在设计过程中,通过处理CT扫描图像,将设备插入真实场景中(图2.11b)。

及其在骨骼中的植入 (b)。(有关此图的彩色表示,请参见彩色 图版部分。))
2.2.5 制造原型
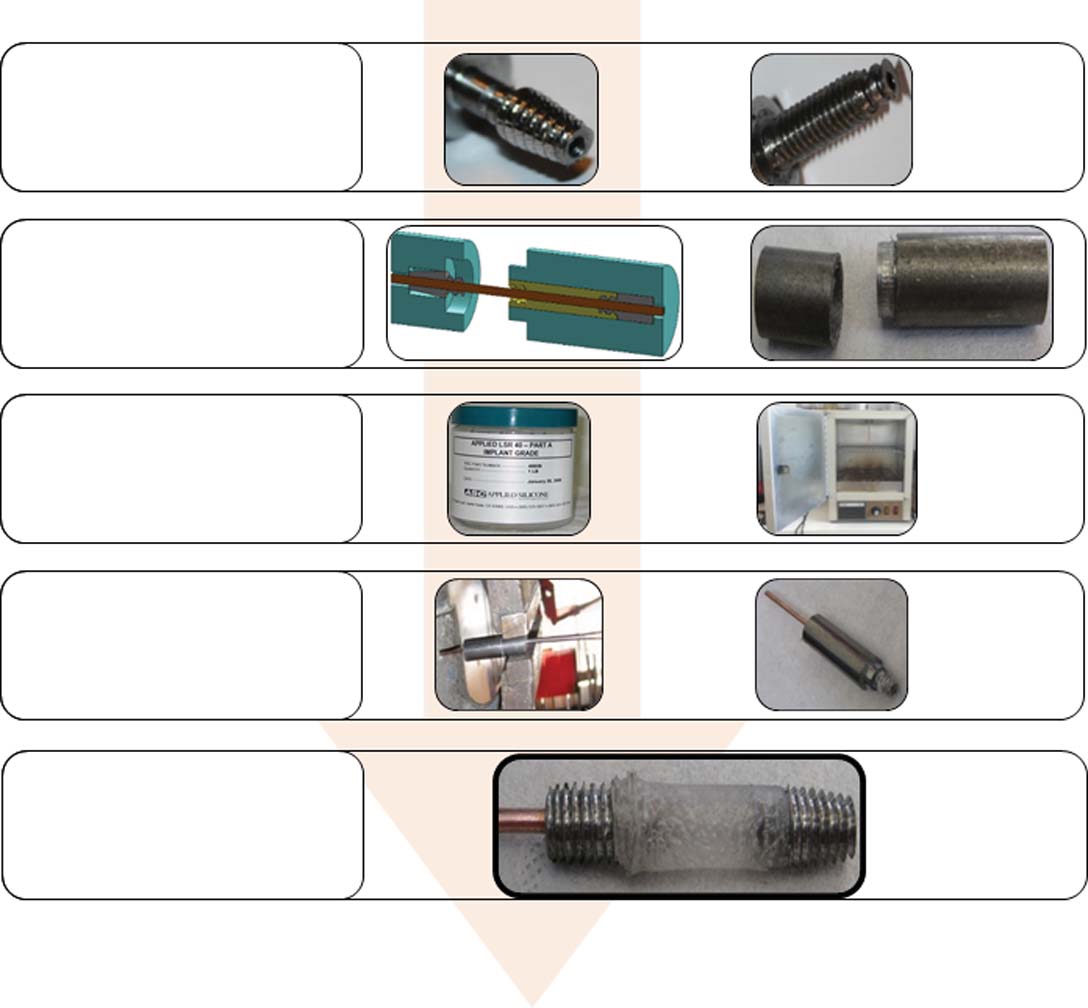
制造该设计的任务总结见图2.12。首先,使用我们实验室现有的牧野车床制造舟骨和月骨部分。考虑到该机床的能力,需要进行多项与制造策略、工具和材料相关的测试,以获得最终部件。接下来,用于浇注包含刚性部件的硅胶的模具也进行了设计和制造。设计了两种不同的版本:矩形和圆柱形。尽管矩形模具似乎更适合浇注过程,但由于在我们实验室中更容易制作,因此选择了圆柱形模具。外部制造模具和其他部件增加了开发时间和产品成本,而作为首个原型,这是不可取的。
在浇注过程中,首先将钛合金部件和克氏针放入模具中;其次,倒入硅胶;第三,关闭模具;最后,将其放入烘箱中以固化硅胶材料。在最后一步中,小心地取出模具,以避免损坏最终假体。
如本节前面所述,该首个原型是使用我们实验室中可用的设备制造的,而这些设备通常专注于中尺度制造。因此,需要进行多项制造测试,且假体的最终质量未达到预期水平。
总之,根据医生的意见,这种新型装置在处理SLIL不稳定性方面具有以下优势:采用刚性和弹性材料的组合,以允许骨骼间的相对距离和骨间位置发生变化;易于植入;以及设计简单(单个部件,避免在手术过程中进行组装)。
此外,应用严谨的系统化设计方法能够获取与该案例研究相关的所有信息和知识,这可用于快速提出其他设计方案,并确保满足客户的需求。尽管这是一种良好的设计方法,但从材料角度来看仍需改进。根据医生的意见,此类硅胶在此情况下并不适用,且无法保证连接的可靠性。
在制造过程中,应使用微制造设备来制造原型。应分析用于最终装配的超声波成型、挤出或注塑等新技术,以及用于刚性部件和模具的微机械加工技术。这样可以更好地加工弹性材料,并更好地实现其与刚性部件的连接。
此外,还需要采用有限元法(FEM)来了解该假体在骨骼中关于运动和载荷方面的精确行为。
2.2.6 气管支架
气管支气管狭窄是指气管通气道的阻塞,可能由多种疾病引起,如恶性或良性肿瘤、气管支气管软化、外部压迫以及插管后气管损伤。对于气管阻塞患者,一种可行的姑息治疗方式是支架置入术[29][30]。这种疗法可立即缓解危及生命的状况,并显著改善患者的生活质量。此外,支架置入术还可作为过渡措施,为后续的治愈性治疗争取时间。目前已有多种不同的气管支架,但尚无完美的形状设计,也缺乏快速简便的制造方法。
本案例研究提出了一种基于一系列设计技术的方法论模型,用于设计功能性和创新性的气管支架,并实现一个参数化工具,该工具能够根据患者参数快速准确地定制最终设计。研究过程中遵循的部分步骤包括
- 气管支架的研究与基准测试,
- 设计开发,
- 对最终支架形状进行参数化以实现定制,
- 材料选择,
- 制造工艺选择,
- 新型气管支架原型的制造。
如本章所述,设计方法论包含用于开发新产品或改进产品的有用工具和技术。在本案例研究中,使用了三种不同的设计工具和一种创新算法,即属性列举法、质量功能展开和发明问题解决理论。
属性列举法关注对象的属性,研究如何改进每个属性。属性包括部件、特性、品质或设计元素,例如尺寸、重量、样式和灵活性。
质量功能展开(QFD)是一种系统化的过程,通过充分理解客户[31]的需求和要求,帮助规划新产品的开发或改进现有产品。QFD 是加强概念设计阶段的有用工具,有助于可视化产品的多种属性,并将其总结为一组称为“质量表”的图表,在这些图表中收集与客户相关的信息[32]。
通过属性列举法得出的属性可以转化为质量功能展开矩阵中的需求项,接着可以通过质量功能展开[31]中的实现方式来确定每一项的技术要求。质量功能展开的技术要求或实现方式代表了工程特性,并从设计师/工程师的角度描述了产品。
需求项与实现方式之间的关系是质量功能展开(QFD)的主体部分,其目的是将客户需求转化为技术特性,从而指导最终产品的设计。所识别出的相互关系通常采用四点量表(高、中、低、无)进行加权,并在矩阵单元格中填入代表该相互关系程度的符号。目标值是QFD最后完成的部分,它总结了从整个矩阵中的数据以及团队讨论中得出的结论,这些目标值是一组新产品需要满足的工程目标值。
TRIZ理论(Teoriya Resheniya Izobretatelskikh Zadatch,俄语)是一种基于科学和技术的发明性问题解决创新算法,需要高度的创造力和创造性[32]。通过分析全球超过150万项专利,TRIZ的开发者发现,所有演化的技术系统都遵循客观规律。这些规律表明,在技术系统的进化过程中,任何功能性能已达到顶峰的系统部分若继续改进,将导致与其他部分的冲突,即出现技术矛盾。克服技术矛盾的工具被称为原理。原理是对在技术系统中执行某一动作以及在系统内部进行操作的通用建议。TRIZ算法中共有40个原理,它们能够为每个技术问题开发出大量解决方案概念。但实施选定的概念仍然是工程师的工作[28]。TRIZ的目的是尽量减少试错次数,而不是提供一种神奇的解决方案。
2.2.7 概念设计
所述设计工具具有使其能够整合的特性,从而使概念设计更加容易,因此更加高效。然而,首先进行了研究和基准分析。
基于广泛的文献研究、支架的基准分析以及从医生和患者处获取的信息,制定出了一份支架理想属性列表。这些属性中的许多都旨在实现支架与患者气管的更好适配性以避免移位,以及实现支架的快速低成本生产,
表2.2 支架属性列表
以及射线不透性等特性。用于制造支架的材料必须具有生物可植入性,以避免任何不良反应。表2.2 显示了这些要求的摘要。
一旦完成属性列表,就很容易找出主要需求项(WHATs),并为每一项建立相应的功能需求(HOWs)[31]。共确定了10项需求,每一项都有一个必须转化为具体数值目标的功能需求(图2.13a)。例如,如果需求是“柔韧性”,则其中一项功能需求可以是“减小壁厚”,其目标值为“小于0.5毫米”。每项需求与所有要求之间均存在强、中、弱或无关联。QFD中的需求项(WHATs)与实现方式(HOWs)展示如图2.13所示。
质量功能展开中需求项与实现方式的展示,以及(b) 质量功能展开竞争分析。)
在质量功能展开(QFD)的竞争分析部分,对六种商用支架设计进行了比较(图2.13b)。竞争分析有助于根据各设计满足需求的程度进行评分—— 5分为最佳,1分为最差。如图2.5所示,满足大多数需求的设计是自然支架和由硅胶制成的杜蒙非扩张型支架。这两种设计在“动态性”和“移位”方面的评分最低;由于两者均由硅胶制成,因此具有柔韧性,但在咳嗽时无法充分改变形状,且容易发生移位。另一方面,与可扩张支架相比,它们更具优势,因为成本较低、插入更方便,并具有优异的生物相容性。
质量功能展开屋顶(QFD roof)汇总了各特性(实现方式)之间的相关性,这些相关性可能是正相关或负相关(图2.14a)。当某一特性得到改进并对另一特性产生期望的影响时,即为强正相关;反之,若对另一特性产生非期望的影响,则为负相关。在质量功能展开屋顶中发现了八个强正相关、七个负相关和六个强负相关;参见图2.14a。
TRIZ原理被应用于已识别的负相关和强负相关,以解决每个矛盾(图2.14b)。
以下是一些示例:
- 原则1(分割:将物体分成独立部分)在本案例中翻译为“分割形状以避免移位”。
- 原理14(曲率:使用曲线表面或形式,而不是直线表面或形式)。
- 原理15(动态性:如果制造过程是刚性的,则使其变为自适应的,将对象分解为能够相互移动的部件),在我们的情况下翻译为“使增材制造技术适应于材料的有效加工”和“在支架上添加不同形状的边缘”。
- 原理3(局部质量:将对象从均匀的变为非均匀的)。
- 原理1(分割:将物体分为不同部分)在本案例中转化为“添加可轻松移动的不同扩口或凸耳以防止移位”和“添加弹簧等其他部件以吸收咳出力”。
- 原理17(另一维度:利用给定区域的另一侧面)在本案例中翻译为“仅在支架的特定部分添加喇叭口或凸起”。
- 原理35(改变浓度或一致性,改变柔韧程度,改变加工或固化温度)。
- 材料必须具有以下特性:适用于长期植入,且具有高弹性模量和邵氏A硬度。
- 原理35(参数变化:改变加工温度,改变材料的物理状态)在本案例中解释为:“如果加工温度难以实现,则可稍后处理材料,或先在一种状态下处理材料,然后再进行改变。”
- 原理27(廉价短寿命物体:使用一次性物体)在我们的案例中解释为: “如果材料无法通过制造技术直接加工,则改变方法,例如使用模具。”
2.2.8 具体化设计和详细设计
TRIZ工程原理被划分为形状解决方案、材料选择和制造技术,并用于为每个领域提供解决方案。这些解决方案将在下文进行说明。
-
形状解决方案
:通过头脑风暴,根据这些发明问题解决理论(TRIZ)方案绘制了大量草图。最终,所有草图都具有三个共同点:类似于气管自然几何形状的D形支架、肌肉壁中减少的材料量,以及每个边缘或环上的圆角。设计头脑风暴后共产生了11个模型(见图2.15),所有设计均经过投票环节。
评分由三位制造领域的专家、四位设计师和四位外科医生完成,评分最高的模型如图2.16所示。该模型的定制参数如下:外径(OD);内径(ID);膜厚度,mt;壁厚,wt;支架长度,L;以及环间距,l。
-
材料解决方案
:材料选择主要要求包括生物相容性和永久植入等级。因此,一种液体长期
在研究了大量材料列表后,选择了植入级铂金硫化硅橡胶(LSR)。
-
制造解决方案
:制造工艺选择质量功能展开表明,为了满足低成本和减少制造的需求,支架必须采用快速成型技术进行制造
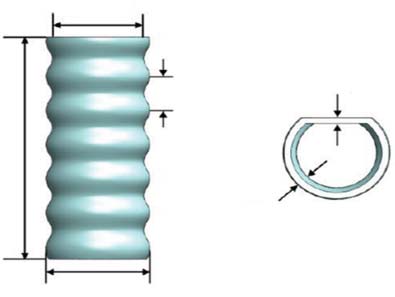
16毫米
60毫米
20毫米
10毫米
(a) (b)
使用 fab@home (b) 直接制造的,一种熔融沉积成型设备。)
小时。由于支气管肺癌患者的预期寿命较低,紧急手术较为频繁,而医院大多数时间标准支架已耗尽,导致在紧急情况下难以及时获得新的支架。例如,使用立体光刻、选择性激光熔化(SLM)、选择性激光烧结(SLS)、熔融沉积成型(FDM)、电子束熔化(EBM)或3D打印等增材制造技术,可在数小时内完成植入物模型的制造并准备进行评估。这些方法及其相关技术正被广泛用于制造定制植入物和假体[30]。最终选择了FDM技术。
2.2.9 制造原型
对于所提出的气管支架设计,已探索了多种制造方法,这些方法均基于增材制造(AM)。首先,为了验证制造概念,使用了非植入性硅胶,并通过商用硅胶和fab@home(一种低成本FDM设备)进行直接制造(图2.17)。为验证制造概念,采用了非植入性硅胶。
然而,长期植入用聚合物(如医用硅胶)相态变化迅速,使用FDM技术对其进行加工非常困难。对于液体硅橡胶材料而言,最合适的加工技术是注塑成型,需考虑采用适配模具来获得该部件,并使用能够注入这种特定材料的技术。
本文所提出的属性列举法、质量功能展开和发明问题解决理论相结合的方法被用于指导一种适用于缓解气道阻塞的新支架设计的开发。
该设计方法论的主要成果包括确定工程要求、生成创新的支架几何结构,以及材料的选择和制造所需技术的确定。作为一个困难的任务,考虑了一些客户需求,例如生物相容性、快速交付和抗移位性。设计了一种波浪形D形支架,旨在避免移位和后壁厚度,这可能增强气管动态功能并防止其发生阻塞。
此外,通过在质量功能展开中整理所有要求,并将发明问题解决理论的概念应用于物理矛盾,材料选择及其制造过程更容易确定。
支架原型的制造可通过增材制造技术实现;然而,所选的生物相容性硅胶无法直接通过这些技术进行处理。因此采用了快速制模方法,并使用熔融沉积成型低成本设备制造和测试了多个模具迭代。模具试验结果表明,提高型腔表面光洁度并在分型线处增加排气通道可改善模具性能。









